O calor de reação é a quantidade de energia liberada ou absorvida durante uma reação química. Ele é uma medida da variação de energia que ocorre durante uma reação, influenciando diretamente na temperatura do sistema. O calor de reação pode ser calculado a partir da diferença entre a energia dos produtos e dos reagentes envolvidos na reação. É uma importante propriedade que ajuda a entender o comportamento das substâncias durante as reações químicas.
Entendendo o calor liberado ou absorvido durante uma reação química.
O calor de reação é a quantidade de calor liberada ou absorvida durante uma reação química. Esse calor pode ser sentido na forma de aumento ou diminuição da temperatura do sistema. Quando uma reação química ocorre, as ligações entre os átomos são quebradas e formadas, resultando em uma liberação ou absorção de energia.
Se a quantidade de energia liberada for maior do que a absorvida, a reação é exotérmica e o sistema libera calor para o ambiente. Por outro lado, se a quantidade de energia absorvida for maior do que a liberada, a reação é endotérmica e o sistema absorve calor do ambiente.
Para medir o calor de reação, é comum utilizar um calorímetro, que é um dispositivo que permite determinar a quantidade de calor envolvida em uma reação química. O calor de reação é representado pela equação:
ΔH = Hprodutos – Hreagentes
Onde ΔH representa a variação de entalpia, Hprodutos é a entalpia dos produtos e Hreagentes é a entalpia dos reagentes. Um valor negativo de ΔH indica que a reação é exotérmica, enquanto um valor positivo indica que a reação é endotérmica.
Em resumo, o calor de reação é uma medida importante para entender o comportamento das reações químicas e a quantidade de energia envolvida. Ele nos ajuda a prever se uma reação liberará ou absorverá calor, e é essencial para o estudo da termodinâmica química.
O que é o calor de solução e como é definido?
O calor de solução é a quantidade de calor liberada ou absorvida quando uma determinada quantidade de soluto é dissolvida em um solvente para formar uma solução. Este processo pode ser exotérmico, liberando calor, ou endotérmico, absorvendo calor.
Para definir o calor de solução, é comum utilizar a equação:
ΔH = q / m
Onde ΔH representa a variação de entalpia, q é a quantidade de calor envolvida no processo e m é a massa do soluto.
É importante destacar que o calor de solução pode influenciar em diversos aspectos, como a temperatura da solução, a velocidade da dissolução e até mesmo na solubilidade de certas substâncias.
Em resumo, o calor de solução é uma medida da energia envolvida no processo de dissolução de um soluto em um solvente, podendo ser tanto liberado quanto absorvido durante essa reação.
Nome da reação que libera energia em forma de calor.
O calor de reação é a quantidade de calor liberada ou absorvida durante uma reação química. Quando uma reação libera energia na forma de calor, ela é chamada de reação exotérmica. Por outro lado, quando uma reação absorve energia na forma de calor, ela é denominada reação endotérmica.
Na reação exotérmica, a energia é liberada para o ambiente na forma de calor. Isso significa que a energia dos produtos é menor do que a energia dos reagentes, resultando em uma diminuição na energia do sistema. Um exemplo comum de uma reação exotérmica é a combustão, onde a queima de um combustível libera calor.
Por outro lado, na reação endotérmica, a energia é absorvida do ambiente na forma de calor. Nesse caso, a energia dos produtos é maior do que a energia dos reagentes, resultando em um aumento na energia do sistema. Um exemplo de uma reação endotérmica é a decomposição do carbonato de cálcio, que requer calor para ocorrer.
Em resumo, o calor de reação é a quantidade de calor liberada ou absorvida durante uma reação química. Quando a energia é liberada na forma de calor, temos uma reação exotérmica, enquanto a energia é absorvida na forma de calor, temos uma reação endotérmica.
Exemplos práticos que ilustram o conceito de entalpia e sua importância na termodinâmica.
A entalpia é uma grandeza termodinâmica que representa a quantidade de energia trocada durante uma reação química a pressão constante. Ela é representada pela letra H e pode ser calculada pela diferença entre a energia interna e o produto da pressão pelo volume do sistema.
Um exemplo prático que ilustra a importância da entalpia na termodinâmica é a combustão do metano (CH4). Nessa reação, o metano reage com o oxigênio (O2) para formar dióxido de carbono (CO2) e água (H2O). Durante essa reação, há uma liberação de energia na forma de calor. O calor de reação, ou entalpia de reação, é a quantidade de energia liberada ou absorvida durante a reação química.
Outro exemplo é a dissolução de cloreto de sódio (NaCl) em água. Nesse caso, a entalpia de dissolução representa a quantidade de energia envolvida na dissolução do sal em água. Se a entalpia de dissolução for positiva, a dissolução é endotérmica, ou seja, absorve calor do ambiente. Se for negativa, a dissolução é exotérmica, liberando calor para o ambiente.
Em resumo, a entalpia é uma grandeza fundamental na termodinâmica que nos permite entender e quantificar a energia envolvida em processos químicos. O calor de reação, representado pela entalpia de uma reação química, é essencial para calcular a quantidade de energia trocada durante uma reação e prever o seu resultado.
O que é calor de reação?
O calor da reacção ou reacção entalpia (AH) é a variação da entalpia de uma reacção química que ocorre a uma pressão constante (Anne Marie Helmenstine, 2014).
Como a entalpia é derivada da pressão, volume e energia interna, que são todas funções do estado, a entalpia também é uma função do estado (Rachel Martin, 2014).
ΔH, ou a mudança de entalpia, surgiu como uma unidade de medida para calcular a mudança de energia de um sistema quando se tornou muito difícil encontrar o ΔU, ou alteração na energia interna de um sistema, medindo simultaneamente a quantidade de calor e trabalho trocado
Dada uma pressão constante, a mudança de entalpia é igual ao calor e pode ser medida como ΔH = q.
A notação ΔHº ou ΔHº r surge então para explicar a temperatura e pressão precisas do calor de reação ΔH.
A entalpia padrão da reação é simbolizada por ΔHº ou ΔHºrxn e pode assumir valores positivos e negativos. As unidades para ΔHº são quiloJoules por mol ou kj / mol.
Conceito anterior para entender o calor da reação: diferenças entre ΔH e ΔHº r .
Δ = representa a alteração na entalpia (entalpia de produtos menos entalpia de reagentes).
Um valor positivo indica que os produtos têm uma entalpia mais alta ou que é uma reação endotérmica (é necessário calor).
Um valor negativo indica que os reagentes têm uma entalpia mais alta ou que é uma reação exotérmica (é produzido calor).
º = significa que a reação é uma alteração de entalpia padrão e ocorre a uma pressão / temperatura predefinida.
r = denota que essa mudança é a entalpia da reação.
O estado padrão: o estado padrão de um sólido ou líquido é a substância pura a uma pressão de 1 bar ou o que é a mesma 1 atmosfera (105 Pa) e a uma temperatura de 25 ° C, ou o que é o mesmo 298 K .
ΔHº r é o calor padrão da reação ou entalpia padrão de uma reação, e como ΔH também mede a entalpia de uma reação. No entanto, ΔHºrxn ocorre em condições “padrão”, o que significa que a reação ocorre a 25 ° C e 1 atm.
O benefício de uma medição de ΔH em condições padrão reside na capacidade de relacionar um valor de ΔHº com outro, uma vez que ocorrem nas mesmas condições (Clark, 2013).
Treino de calor
O calor padrão de formação, ΔH f º, de um produto químico é a quantidade de calor absorvido ou liberado pela formação de 1 mole desse produto químico a 25 graus Celsius e 1 bar de seus elementos em seus estados padrão.
Um elemento está em seu estado padrão se estiver em sua forma mais estável e em seu estado físico (sólido, líquido ou gás) a 25 graus Celsius e 1 bar (Jonathan Nguyen, 2017).
Por exemplo, o calor de formação padrão para dióxido de carbono envolve oxigênio e carbono como reagentes.
O oxigénio é mais estável que as moléculas de gás ó 2 , enquanto o carbono é mais estável como uma grafite sólida. (A grafite é mais estável que o diamante em condições padrão.)
Para expressar a definição de outra maneira, o calor padrão da formação é um tipo especial de calor padrão da reação.
A reação é a formação de 1 mole de uma substância química de seus elementos em seus estados padrão em condições padrão.
O calor padrão do treinamento também é chamado de entalpia padrão do treinamento (embora realmente seja uma mudança na entalpia).
Por definição, a formação de um elemento em si não produziria nenhuma alteração na entalpia; portanto, o calor padrão da reação para todos os elementos é zero (Cai, 2014).
Cálculo de entalpia de reação
1- Cálculo experimental
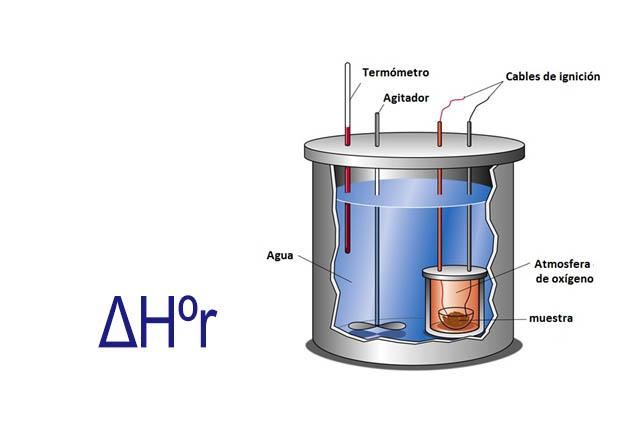
A entalpia pode ser medida experimentalmente usando um calorímetro. Um calorímetro é um instrumento em que uma amostra é reagida através de fios elétricos que fornecem a energia de ativação. A amostra está em um recipiente cercado por água, que é constantemente agitada.
Medindo-se uma mudança de temperatura que ocorre quando a amostra é reagida e conhecendo o calor específico da água e sua massa, o calor que libera ou absorve a reação é calculado usando a equação q = Cesp xmx ΔT.
Nesta ação q é calor, Cesp é o calor específico neste caso de água que é igual a 1 caloria por grama, m é a massa de água e ΔT é a mudança de temperatura.
O calorímetro é um sistema isolado que tem pressão constante, então ΔH r = q
2- Cálculo teórico
A mudança de entalpia não depende da rota específica de uma reação, mas apenas do nível geral de energia dos produtos e reagentes. A entalpia é uma função do estado e, como tal, é aditiva.
Para calcular a entalpia padrão de uma reação, podemos adicionar as entalpias padrão da formação de reagentes e subtraí-la da soma das entalpias padrão da formação do produto (Boundless, SF). Matematicamente dito, isso nos dá:
ΔH r ° = Σ ΔH f º (produtos) – Σ ΔH f º (reagentes).
As entalpias das reações são geralmente calculadas a partir das entalpias da formação de reagentes em condições normais (pressão de 1 bar e temperatura de 25 graus Celsius).
Para explicar esse princípio da termodinâmica, calcularemos a entalpia da reação para a combustão de metano (CH 4 ) de acordo com a fórmula:
CH 4 (g) + 2O 2 (g) → CO 2 (g) + 2H 2 O (g)
Para calcular a entalpia padrão da reação, precisamos procurar as entalpias padrão da formação de cada um dos reagentes e produtos envolvidos na reação.
Estes são geralmente encontrados em um apêndice ou em várias tabelas online. Para esta reação, os dados que precisamos são:
H f º CH 4 (g) = -75 kjoul / mol.
H f º O 2 (g) = 0 kjoul / mol.
H f º CO 2 (g) = -394 kjoul / mol.
H f ° H 2 O (g) = -284 kjoul / mol.
Observe que, como está em seu estado padrão, a entalpia padrão de formação para gás oxigênio é 0 kJ / mol.
Abaixo, resumimos nossas entalpias padrão de treinamento. Observe que, como as unidades estão em kJ / mol, precisamos multiplicar pelos coeficientes estequiométricos na equação da reação balanceada (Leaf Group Ltd, SF).
F ΔH f º (produtos) = ΔH f º CO 2 +2 ΔH f º H 2 O
F ΔH f º (produtos) = -1 (394 kjoul / mol) -2 (284 kjoul / mol) = -962 kjoul / mol
F ΔH f º (reagentes) = ΔH f º CH 4 + ΔH f º O 2
F ΔH f º (reagentes) = -75 kjoul / mol + 2 (0 kjoul / mol) = -75 kjoul / mol
Agora, podemos encontrar a entalpia padrão da reação:
ΔH r ° = Σ ΔH f º (produtos) – Σ ΔH f º (reagentes) = (- 962) – (- 75) =
ΔH r ° = – 887kJ / mol.
Referências
- Anne Marie Helmenstine. (11 de junho de 2014). Entalpia da definição de reação. Recuperado da thoughtco: thoughtco.com.
- (SF). Entalpia padrão de reação. Recuperado de ilimitado: boundless.com.
- Cai, E. (2014, 11 de março). calor padrão de formação. Recuperado de chemicalstatistician: chemicalstatistician.wordpress.com.
- Clark, J. (2013, maio). Várias definições de mudança de entalpia. Recuperado de chemguide.co.uk: chemguide.co.uk.
- Jonathan Nguyen, GL (2017, 9 de fevereiro). Entalpia padrão de formação. Recuperado de chem.libretexts.org: chem.libretexts.org.
- Grupo Folha Ltd. (SF). Como calcular entalpias de reação. Recuperado de sciencing: sciencing.com.
- Rachel Martin, EY (2014, 7 de maio). Calor de Reação Recuperado de chem.libretexts.org: chem.libretexts.org.