- O câncer de mama é o tumor mais frequente nas mulheres, com incidência em alta, mas mortalidade em queda graças ao rastreio e aos tratamentos modernos.
- Fatores de risco incluem idade, genética, hormonas, estilo de vida e desigualdades de acesso, com forte impacto em grupos raciais e etários específicos.
- Os subtipos moleculares, o estadiamento TNM e marcadores como HER2 e receptores hormonais orientam terapias cada vez mais personalizadas.
- Novas estratégias como terapias dirigidas, imunoterapia e biópsia líquida estão a transformar o prognóstico, inclusive na doença metastática.
O câncer de mama continua a ser o tumor mais diagnosticado em mulheres em todo o mundo e, apesar de todos os avanços, ainda representa um enorme desafio de saúde pública. Estima-se que quase 2,3 milhões de mulheres recebam esse diagnóstico a cada ano, o que torna fundamental entender bem as estatísticas mais recentes, os fatores de risco, as opções de detecção precoce e o impacto dos tratamentos modernos na sobrevivência.
Em países como Espanha, Estados Unidos e no conjunto da União Europeia, os dados mostram uma realidade paradoxal: a incidência (ou seja, o número de novos casos) segue em alta, enquanto as taxas de mortalidade tendem a cair graças ao diagnóstico precoce e às terapias cada vez mais personalizadas. Conhecer esses números ajuda não apenas a dimensionar o problema, mas também a tomar decisões mais conscientes sobre rastreio, estilo de vida e acompanhamento médico.
Estatísticas globais e panorama em Espanha
O câncer de mama é hoje o tipo de câncer mais frequentemente diagnosticado no mundo, e ocupa aproximadamente o quinto lugar em mortalidade global por câncer. De acordo com a International Agency for Research on Cancer (IARC), em torno de 2,3 milhões de mulheres desenvolvem tumores malignos de mama a cada ano, consolidando a doença como uma prioridade absoluta em saúde pública.
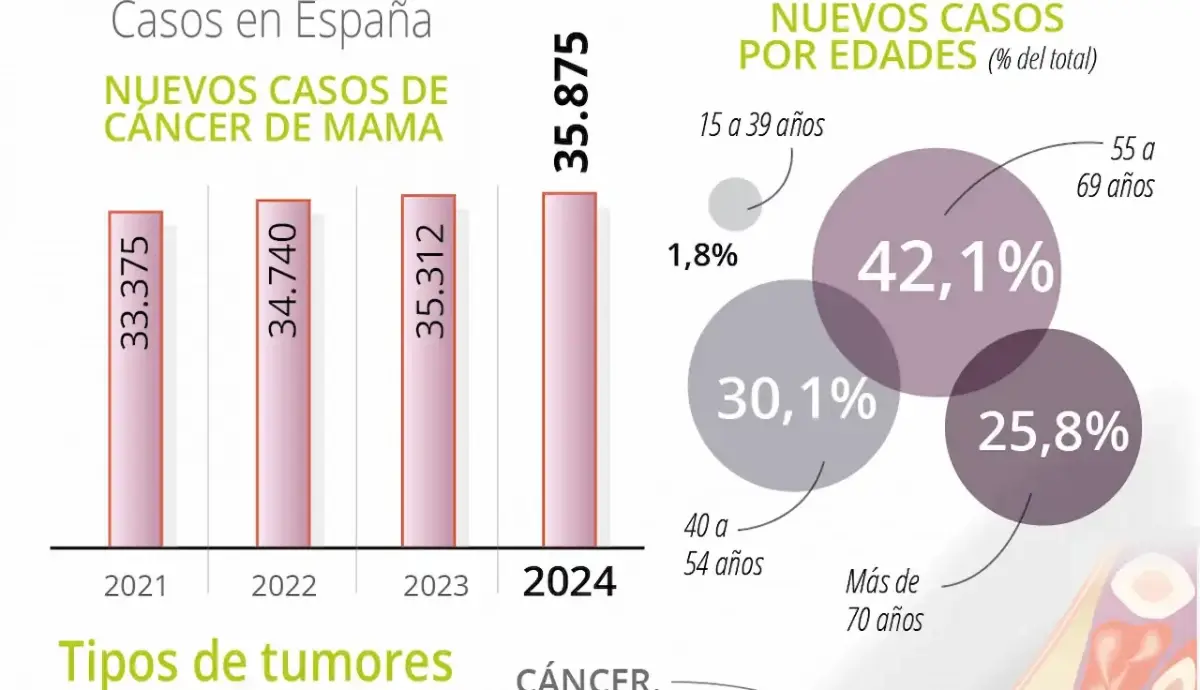
Em Espanha, as projeções para 2025 apontam para cerca de 37.682 novos casos de câncer de mama, mantendo-se como o tumor mais comum entre as mulheres espanholas. As estimativas indicam que 1 em cada 8 mulheres no país terá câncer de mama em algum momento da vida, um risco muito semelhante ao calculado para outras populações ocidentais.
A sobrevivência, no entanto, melhorou de forma notável nas últimas décadas. Em Espanha, a taxa de sobrevivência global situa-se em torno de 85,5%, enquanto na Catalunha chega a aproximadamente 89,8%. Esses números refletem o impacto positivo dos programas de rastreio (mamografia) e da incorporação de terapias cirúrgicas, radioterápicas e sistêmicas cada vez mais eficazes.
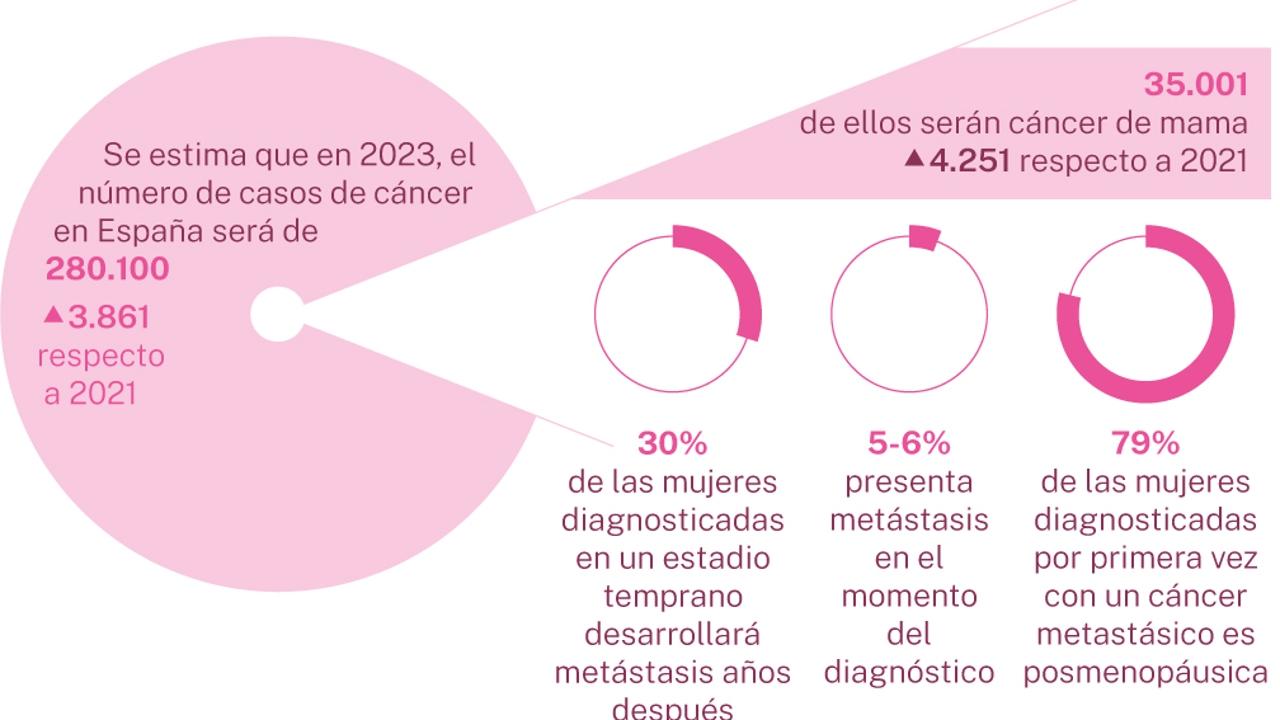
O câncer de mama masculino continua a ser raro, representando cerca de 1% de todos os casos, mas merece atenção porque costuma ser diagnosticado em fases mais avançadas e menos esperadas. Além disso, dentro do universo dos diagnósticos femininos, entre 5% e 6% das mulheres já apresentam doença metastática ao diagnóstico e, ao longo da evolução, entre 20% e 30% acabam desenvolvendo metástases, uma situação que hoje ainda não é curável e se associa a uma sobrevivência média em torno de cinco anos.
Incidência, mortalidade e tendências recentes
Nos Estados Unidos, calcula-se que cerca de 1 em cada 8 mulheres (aproximadamente 13%) desenvolverá câncer de mama invasivo ao longo da vida. Embora o risco individual permaneça elevado, a mortalidade global caiu graças à combinação de rastreio organizado, terapias modernas e maior consciência sobre sintomas precoces.
Mesmo assim, a incidência segue aumentando de forma lenta, mas constante. Entre 2012 e 2021, a taxa de novos casos de câncer de mama nos EUA cresceu cerca de 1% ao ano. O aumento é ainda mais marcado em mulheres com menos de 50 anos, com incrementos anuais de aproximadamente 1,4%, e em grupos étnicos como hispânicas (1,6% ao ano) e mulheres asiático-americanas e das ilhas do Pacífico (até 2,6% ao ano).
As projeções norte-americanas para 2026 sugerem cerca de 321.910 novos casos de câncer de mama invasivo em mulheres, aos quais se somariam em torno de 60.730 diagnósticos de carcinoma ductal in situ (CDIS), um tipo de tumor não invasivo. Estima-se ainda que pouco mais de 16% das mulheres diagnosticadas tenham menos de 50 anos, confirmando a tendência de aumento em idades mais jovens.
Cerca de 66% dos casos de câncer de mama são detectados ainda em fase localizada, antes da disseminação para fora da mama, momento em que o tratamento costuma ser mais eficaz e as possibilidades de cura são muito altas. Em contrapartida, aproximadamente 42.140 mulheres deverão morrer por câncer de mama em 2026 nos EUA, o que mostra que ainda há um caminho relevante a percorrer.
Na União Europeia e no Reino Unido, as tendências de mortalidade são em geral favoráveis. As estimativas para 2025 apontam para uma queda global de 4% nas taxas de mortalidade por câncer de mama na UE e de cerca de 6% no Reino Unido, em comparação com 2020, quando ajustadas por idade (taxa de mortalidade padronizada).
Em números absolutos, isso se traduz em aproximadamente 90.100 mortes por câncer de mama previstas na UE em 2025, correspondendo a uma taxa padronizada em torno de 13,3 óbitos por 100.000 mulheres. No Reino Unido, projeta-se uma taxa muito semelhante, de 13,2 óbitos por 100.000 mulheres, o que significaria cerca de 11.400 mortes.
Os dados por país mostram reduções muito relevantes: na Alemanha espera-se uma queda de cerca de 14% na mortalidade por câncer de mama, no Reino Unido em torno de 10%, na Polónia aproximadamente 9%, enquanto França e Espanha registrariam quedas em torno de 8%, e a Itália em torno de 2%. Entre 1989 e 2025, estima-se que cerca de 373.000 mortes por câncer de mama tenham sido evitadas na UE e 197.000 no Reino Unido, graças sobretudo a melhorias no tratamento e, em menor proporção (25%-30%), à expansão do rastreio mamográfico.
Um dado que chama a atenção é o comportamento por faixa etária. Na UE, antecipa-se que as taxas de mortalidade diminuam entre 7% e 12% em quase todos os grupos etários, exceto entre mulheres com 80 anos ou mais, nas quais se espera um aumento de quase 10% na mortalidade. Pesquisadores sugerem que, nessa faixa, muitas mulheres fazem rastreio com menos frequência e nem sempre recebem terapias inovadoras, somando-se a um aumento de obesidade e sobrepeso que eleva o risco de câncer de mama.
Disparidades raciais, étnicas e por idade
Apesar da melhoria global das estatísticas, as desigualdades entre grupos raciais e étnicos continuam marcantes. Nos Estados Unidos, por exemplo, as mulheres negras têm maior probabilidade de morrer por câncer de mama do que qualquer outro grupo racial ou étnico, mesmo quando o acesso teórico aos tratamentos é semelhante.
Curiosamente, a incidência de câncer de mama em mulheres negras é cerca de 5% menor do que em mulheres brancas, mas o risco de morte é aproximadamente 38% mais alto. Em mulheres nativas da América do Norte e do Alasca, observa-se um padrão semelhante: incidência cerca de 10% menor que a de mulheres brancas, mas risco de morte aproximadamente 6% superior, sugerindo diferenças em diagnóstico precoce, acesso, adesão ou qualidade terapêutica.
As disparidades também se manifestam em outros grupos específicos. Mulheres de ascendência judaica asquenazita, por exemplo, apresentam risco maior de câncer de mama devido a uma frequência aumentada de mutações em genes como BRCA1 e BRCA2. Além disso, homens negros exibem as maiores taxas de incidência e mortalidade por câncer de mama masculino, embora o câncer de mama em homens represente menos de 1% de todos os casos.
A idade ao diagnóstico é outro fator crítico. A idade média ao receber o diagnóstico de câncer de mama situa-se em torno de 62 anos; isto significa que metade das pacientes é diagnosticada antes dos 62 e a outra metade depois. No entanto, o número de casos em mulheres jovens vem aumentando: estimativas para 2024 indicam que cerca de 16% das mulheres com câncer de mama têm menos de 50 anos, o que desafia a ideia de que se trata exclusivamente de uma doença da pós-menopausa.
No contexto espanhol, a idade de maior incidência está acima dos 50 anos, mas em torno de 10% dos casos são diagnosticados em mulheres com menos de 40 anos. Em muitos países europeus, vem sendo documentado um aumento da incidência em idades mais jovens, algo que ainda está a ser estudado em detalhe em Espanha, mas que já levanta preocupações entre oncologistas e especialistas em saúde pública.
Fatores de risco, genética e câncer de mama hereditário
O câncer de mama é uma doença de origem multifatorial, ou seja, resulta da interação complexa entre fatores genéticos, hormonais, reprodutivos, ambientais e de estilo de vida. Em grande parte dos casos não é possível apontar uma causa única, mas conhecemos bem diversos fatores de risco modificáveis e não modificáveis.
Entre os fatores não modificáveis, a idade é o mais importante: o risco aumenta progressivamente com o envelhecimento. Também pesam o histórico pessoal de câncer de mama (quem já teve um tumor de mama invasivo ou carcinoma ductal in situ tem maior probabilidade de desenvolver um novo câncer, inclusive na outra mama), bem como certas lesões benignas de alto risco, como a hiperplasia ductal atípica.
A densidade mamária elevada na mamografia é outro fator conhecido, tanto porque aumenta o risco biológico em si como porque pode dificultar a detecção de tumores pela imagem. Além disso, uma história menstrual longa (menarca precoce e menopausa tardia) implica exposição hormonal prolongada, o que eleva o risco.
A exposição a radiações ionizantes, especialmente na adolescência e juventude, é outro fator relevante, assim como mutações genéticas herdadas em genes como BRCA1, BRCA2, PALB2, TP53, PTEN, ATM, CHEK2, entre outros. As mutações de BRCA1/2 são responsáveis por cerca de 20% a 25% dos cânceres de mama hereditários, e mulheres portadoras podem ter um risco cumulativo superior a 50%-70% até os 70 anos, dependendo do gene envolvido.
Mesmo assim, a maioria dos casos de câncer de mama não está ligada à herança direta. Cerca de 5% a 10% de todos os cânceres de mama são considerados hereditários, enquanto aproximadamente 85% ocorrem em mulheres sem histórico familiar importante, resultado de mutações adquiridas ao longo da vida associadas ao envelhecimento e a exposições diversas.
Entre os fatores de risco modificáveis, vários se relacionam com o padrão reprodutivo e o estilo de vida. A nuliparidade (nunca ter engravidado), o primeiro parto após os 30 anos, a ausência de amamentação e o uso prolongado de terapia hormonal de substituição na menopausa ou de contraceptivos orais aumentam discretamente o risco. O consumo de álcool, o sobrepeso e a obesidade (especialmente após a menopausa), o sedentarismo e uma dieta pobre, distante do padrão mediterrânico, também contribuem para elevar a probabilidade de desenvolver a doença.
Outro aspecto importante é a identidade de género e terapias hormonais em pessoas trans e não binárias. Quem recebe hormônios feminilizantes ou tem mamas desenvolvidas deve discutir com a equipa médica o nível de risco e as estratégias de rastreio mais adequadas, uma vez que as recomendações tradicionais foram pensadas para mulheres cisgénero e precisam ser ajustadas a novas realidades.
Estrutura da mama, definição e características do tumor
Para entender melhor o câncer de mama, vale lembrar rapidamente como é a anatomia mamária. A mama é composta por 10 a 20 lóbulos, que se dividem em unidades menores chamadas lobulílios, onde se produz o leite durante a amamentação. Esse leite percorre ductos até alcançar o mamilo. O espaço entre lobulílios e ductos é preenchido por tecido gorduroso e fibroso, além de uma rede de vasos linfáticos que drenam, sobretudo, para os gânglios axilares.
O câncer de mama surge quando células do epitélio glandular começam a proliferar de maneira descontrolada, perdendo os mecanismos normais de reparação e morte celular. Essas células podem permanecer confinadas aos ductos ou lobulílios (tumores in situ) ou atravessar suas paredes e invadir o tecido vizinho (tumores invasivos). Ao ganhar acesso a vasos sanguíneos ou linfáticos, podem alcançar outros órgãos e formar metástases.
Do ponto de vista histológico, o tipo mais comum é o carcinoma ductal, que representa cerca de 80% dos casos e se origina nos ductos por onde flui o leite. O carcinoma lobular é o segundo mais frequente, partindo dos lobulílios. O patologista também avalia o grau histológico, que indica quão diferenciadas estão as células: tumores de grau I são mais parecidos com o tecido normal e, em geral, menos agressivos, enquanto grau III indica células mais imaturas e de maior potencial de crescimento.
Além disso, são analisados marcadores fundamentais como receptores hormonais, HER2, Ki-67 e outros biomarcadores moleculares. A expressão de receptores de estrogênio e progesterona indica que o tumor é, potencialmente, sensível à hormonoterapia e costuma associar-se a melhor prognóstico. Já a superexpressão de HER2, presente em 15%-20% dos casos, antes era um marcador de agressividade, mas hoje se tornou também um alvo terapêutico graças a anticorpos específicos.
O índice de proliferação Ki-67 mostra a percentagem de células em divisão ativa; valores elevados sugerem comportamento mais agressivo. Sobre a peça cirúrgica, o patologista descreve também o tamanho tumoral, o número de gânglios axilares comprometidos e o estado das margens cirúrgicas (se estão livres ou não de tumor), todos elementos decisivos para definir o prognóstico e a necessidade de tratamentos adicionais.
Classificação molecular, estadiamento e fatores prognósticos
Com o avanço das técnicas moleculares, o câncer de mama passou a ser classificado também por subtipos intrínsecos, que combinam dados de expressão génica e imunohistoquímica. De forma simplificada, fala-se em tumores Luminal A, Luminal B (HER2 negativo ou positivo), HER2-enriched e basal-like ou triplo negativo. Em geral, os tumores luminais expressam receptores hormonais, os HER2-enriched têm alta expressão de HER2 e os basal-like não expressam nem receptores hormonais nem HER2.
O subtipo molecular tem impacto direto no prognóstico e na escolha do tratamento. Em linhas gerais, os tumores Luminal A tendem a ter melhor prognóstico, crescimento mais lento e boa resposta à hormonoterapia, enquanto os triplo negativos e alguns HER2-enriched são mais agressivos, com maior risco de recaída precoce, exigindo abordagens sistémicas mais intensas.
O estadiamento segue a classificação TNM, que considera o tamanho do tumor primário (T), o estado dos gânglios linfáticos regionais (N) e a presença ou não de metástases à distância (M). Estádios iniciais (I e II) correspondem a tumores limitados à mama e, no máximo, a poucos gânglios; estádios localmente avançados (III) envolvem tumores grandes, pele ou cadeia ganglionar extensa; e o estádio IV indica doença metastática.
Algumas variantes, como o câncer de mama inflamatório, merecem menção especial. Nesse subtipo, as células tumorais bloqueiam os vasos linfáticos da pele da mama, que passa a apresentar vermelhidão, calor, inchaço e aspecto de “pele de laranja”. Costuma corresponder a estádios avançados (IIIB, IIIC ou IV) e exige tratamento sistêmico intensivo combinado com cirurgia e radioterapia.
Os principais fatores prognósticos incluem tamanho tumoral, número de gânglios comprometidos, grau histológico, expressão de receptores hormonais e HER2, além do subtipo molecular. O envolvimento linfonodal axilar, por exemplo, é um dos indicadores mais fortes de risco de recaída: quanto maior o número de gânglios afetados, maior a probabilidade de recidiva. Enquanto isso, a expressão de receptores hormonais prevê boa resposta à hormonoterapia, e a presença de HER2 superexpresso indica benefício com terapias anti-HER2 como o trastuzumab.
Em Espanha, a sobrevivência a 5 anos em tumores em estádio I supera 98%, mas cai para cerca de 24% nos estádios IV, ilustrando a importância crucial do diagnóstico precoce e do acesso rápido a tratamentos completos em centros especializados.
Deteção precoce, rastreio e sintomas de alerta
O diagnóstico precoce é uma das chaves que explicam a queda nas taxas de mortalidade. A mamografia se consolidou como o exame de rastreio mais eficaz para mulheres de risco médio, permitindo identificar tumores milimétricos, muitas vezes antes de qualquer sintoma.
Em Espanha, todas as comunidades autónomas implementaram programas de rastreio populacional por mamografia, geralmente dirigidos a mulheres entre 50 e 69 anos, com convites a cada dois anos. Em mulheres de alto risco (história familiar forte, mutações genéticas, etc.), as recomendações mudam: costuma-se começar mais cedo, com exames mais frequentes e, às vezes, associando ressonância magnética da mama ao rastreio.
Mesmo com o rastreio organizado, é essencial estar atenta a sinais clínicos. O sintoma mais comum é o aparecimento de um nódulo palpável, de consistência firme e, em geral, indolor. Outros sinais incluem retração do mamilo, alterações da pele (vermelhidão, aspeto de casca de laranja, feridas que não cicatrizam), secreção mamilar anormal e presença de gânglios aumentados na axila. Grande parte desses achados acaba correspondendo a doenças benignas, mas é crucial que qualquer alteração persistente seja avaliada por ginecologista ou mastologista.
A investigação diagnóstica combina exame clínico com métodos de imagem como mamografia, ecografia e, quando indicado, ressonância magnética. O diagnóstico definitivo, porém, exige sempre uma biópsia, geralmente por agulha grossa guiada por palpação ou imagem, para analisar o tecido ao microscópio e definir o tipo de tumor, grau, marcadores e outros parâmetros decisivos.
Em estádios mais avançados, são necessários exames adicionais para avaliar a extensão da doença, como tomografia computadorizada (TAC), gammagrafia óssea ou tomografia por emissão de positrões (PET), entre outros. Em casos selecionados, a PET pode substituir alguns exames ou resolver dúvidas em relação a metástases em órgãos específicos.
Tratamentos: cirurgia, radioterapia e terapias sistémicas
O tratamento do câncer de mama é cada vez mais individualizado, levando em conta estádio, subtipo molecular, idade, condições gerais da paciente, preferências pessoais e presença ou não de mutações genéticas. Em estádios iniciais, costuma-se combinar cirurgia com radioterapia e algum tipo de terapia sistémica (quimioterapia, hormonoterapia, terapias dirigidas e, em certos casos, imunoterapia).
Do ponto de vista cirúrgico, existem duas grandes opções em tumores localizados: a cirurgia conservadora, na qual se remove apenas o tumor com uma margem de tecido saudável, preservando a maior parte da mama, e a mastectomia, que consiste na remoção completa da mama. A decisão depende de fatores como tamanho tumoral, localização, volume mamário, presença de múltiplos focos e desejo da paciente. Após a mastectomia, podem ser oferecidas diversas técnicas de reconstrução imediata ou diferida, com implantes ou tecidos próprios.
A avaliação dos gânglios da axila é parte crucial do tratamento cirúrgico. Quando não há sinais claros de envolvimento ganglionar, utiliza-se a técnica do gânglio sentinela, em que se injeta um corante ou substância radioativa perto do tumor para identificar o primeiro gânglio de drenagem. Se esse gânglio não contém células tumorais, evita-se a linfadenectomia completa, reduzindo significativamente o risco de linfedema (inchaço crónico do braço) e outras complicações.
A radioterapia é frequentemente usada como tratamento adjuvante após cirurgia conservadora, e em muitos casos depois da mastectomia, sobretudo quando há tumores grandes ou gânglios positivos. As técnicas modernas (planeamento 3D, radioterapia de intensidade modulada, radioterapia guiada por imagem, hipofracionamento e radioterapia intraoperatória) permitem entregar doses elevadas ao leito tumoral, poupando coração, pulmões e tecidos saudáveis, com menos sessões e menos efeitos colaterais do que há algumas décadas.
As terapias sistémicas englobam quimioterapia, hormonoterapia, terapias dirigidas, imunoterapia e fármacos de suporte. A quimioterapia utiliza combinações de fármacos como antraciclinas, taxanos, capecitabina, platinos, eribulina e outros para destruir células com alto índice de proliferação. Pode ser administrada antes da cirurgia (neoadjuvante) para reduzir o tumor e avaliar a resposta, ou depois (adjuvante) para eliminar micrometástases invisíveis.
A hormonoterapia é pilar central nos tumores com receptores hormonais positivos. Em mulheres na pré-menopausa, utiliza-se com frequência tamoxifeno e, em pacientes de alto risco, bloqueio da função ovárica com análogos da hormona libertadora de gonadotropina. Na pós-menopausa, predominam os inibidores da aromatase (anastrozol, letrozol, exemestano). Cada vez mais, combinam-se esses agentes com inibidores de CDK4/6 (palbociclib, ribociclib, abemaciclib), tanto na doença metastática como, em determinados cenários, no contexto adjuvante.
As terapias dirigidas transformaram o prognóstico dos tumores HER2 positivos e de alguns subtipos luminais. Anticorpos como trastuzumab e pertuzumab, e conjugados anticorpo-fármaco como T-DM1 (ado-trastuzumab emtansina) e trastuzumab deruxtecano, aumentaram de forma impressionante a sobrevivência em doença localizada e metastática. Outros fármacos atuam em vias de sinalização específicas, como inibidores de PI3K, AKT e mTOR (alpelisib, inavolisib, capivasertib, everolimus), especialmente em tumores com mutações nessa rota.
Para pacientes portadoras de mutações BRCA1/2, os inibidores de PARP (como olaparib e talazoparib) representam uma estratégia fundamental, pois exploram a deficiência de reparo de DNA dessas células tumorais, levando-as à morte seletiva. Esses fármacos são utilizados tanto em doença metastática como em determinados contextos adjuvantes de alto risco.
A imunoterapia, por sua vez, ganhou espaço sobretudo no câncer de mama triplo negativo. Medicamentos como pembrolizumab e atezolizumab, que bloqueiam pontos de controlo imunológico, podem ser combinados com quimioterapia em estádios avançados e, em alguns casos, também na fase neoadjuvante, melhorando a taxa de resposta patológica completa e o controlo de longo prazo.
Doença metastática, novos avanços e seguimento a longo prazo
Quando o câncer de mama atinge o estádio IV, com metástases em órgãos distantes (osso, fígado, pulmões, cérebro, entre outros), o objetivo principal do tratamento deixa de ser curativo e passa a ser prolongar a vida com a melhor qualidade possível. Nessa fase, a escolha entre hormonoterapia, quimioterapia, terapias dirigidas, imunoterapia e cuidados de suporte é feita com base no subtipo tumoral, nas terapias já utilizadas e nas preferências da paciente.
Nas últimas décadas, os resultados em doença metastática melhoraram de forma consistente. Combinações como inibidores de CDK4/6 com hormonoterapia prolongam a sobrevivência em anos em tumores luminais. Em triplo negativo, conjugados anticorpo-fármaco como sacituzumab govitecan e, mais recentemente, moléculas como datopotomab deruxtecano (em fase de aprovação em vários países), oferecem novas opções após múltiplas linhas de tratamento.
Outras frentes de investigação incluem terapias celulares, vacinas antitumorais e uso extensivo de biópsia líquida. Ensaios com linfócitos infiltrantes de tumor (TILs) e células CAR-T específicas para alvos mamários estão em andamento, ainda em fases iniciais. Vacinas experimentais buscam “treinar” o sistema imune para reconhecer e atacar células residuais, reduzindo o risco de recaída.
A biópsia líquida, que detecta fragmentos de DNA tumoral circulante no sangue, é uma das tecnologias mais promissoras para monitorizar doença residual mínima e ajustar o tratamento em tempo real. Estudos avaliam se a identificação precoce de DNA tumoral após terapias curativas em tumores de alto risco pode justificar intervenções adicionais antes que surjam metástases visíveis.
O seguimento após o tratamento de estádios precoces é igualmente essencial. Recomenda-se, em geral, consultas a cada 4-6 meses nos primeiros cinco anos, e depois anuais, com exame físico e mamografia anual da mama remanescente e da contralateral. Em pacientes que utilizam tamoxifeno, orienta-se realizar revisão ginecológica anual devido ao risco ligeiramente aumentado de câncer de endométrio, enquanto mulheres em uso de inibidores da aromatase devem fazer densitometrias periódicas para monitorizar a saúde óssea.
As terapias sistémicas englobam quimioterapia, hormonoterapia, terapias dirigidas, imunoterapia e fármacos de suporte. A quimioterapia utiliza combinações de fármacos como antraciclinas, taxanos, capecitabina, platinos, eribulina e outros para destruir células com alto índice de proliferação. Pode ser administrada antes da cirurgia (neoadjuvante) para reduzir o tumor e avaliar a resposta, ou depois (adjuvante) para eliminar micrometástases invisíveis.
Estilos de vida saudáveis fazem parte do plano de sobrevivência. Evitar ganho de peso, praticar atividade física regular, limitar o álcool e manter uma dieta equilibrada, de tipo mediterrânico, estão associados a melhor prognóstico e menor risco de recaída, sendo hoje considerados componentes fundamentais do cuidado oncológico moderno.
O cenário atual do câncer de mama combina números ainda elevados de incidência com uma notável redução da mortalidade, graças ao rastreio sistemático, à sensibilização da população, à integração de equipas multidisciplinares e a uma verdadeira revolução terapêutica que vai da cirurgia conservadora aos fármacos dirigidos mais sofisticados. Ainda que o desafio da doença metastática e das disparidades de acesso persista, o ritmo acelerado da investigação – com Espanha e outros países europeus entre os líderes em ensaios clínicos – permite olhar para o futuro com um otimismo cauteloso, apostando em diagnósticos cada vez mais precoces, tratamentos mais personalizados e sobreviventes que possam viver mais e melhor depois de um diagnóstico de câncer de mama.