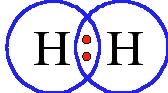
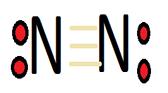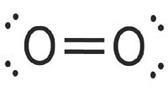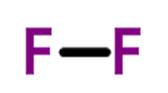Os elementos diatômicos são aqueles que em sua forma elementar se apresentam como moléculas compostas por dois átomos iguais. Isso significa que, ao contrário dos elementos monoatômicos, que são formados por átomos isolados, os elementos diatômicos estão ligados por uma ligação covalente. Alguns exemplos de elementos diatômicos comuns são o oxigênio (O2), o nitrogênio (N2) e o hidrogênio (H2). A presença de dois átomos na molécula confere propriedades específicas a esses elementos, que podem se manifestar de formas diversas em diferentes condições.
Conheça as moléculas formadas por dois átomos presentes na natureza e suas características.
Os elementos diatômicos são moléculas formadas por dois átomos presentes na natureza. Alguns exemplos destes elementos são o oxigênio (O2), o nitrogênio (N2), o hidrogênio (H2) e o flúor (F2).
Cada uma dessas moléculas possui características únicas. Por exemplo, o oxigênio é um gás incolor, inodoro e insípido que é essencial para a respiração e combustão. O nitrogênio, por sua vez, é um gás incolor e inodoro que compõe a maior parte da atmosfera terrestre e é crucial para a vida na Terra.
O hidrogênio é o elemento mais abundante no universo e é um gás inflamável. Já o flúor é um elemento altamente reativo e corrosivo, sendo utilizado em várias aplicações industriais.
Portanto, os elementos diatômicos são moléculas com propriedades distintas e desempenham papéis importantes na natureza e na indústria.
Tipos de moléculas: conheça as diferentes categorias de compostos químicos presentes na natureza.
Existem diversos tipos de moléculas presentes na natureza, cada uma com suas características e propriedades únicas. Uma das categorias de compostos químicos são os elementos diatômicos, ou seja, moléculas formadas por dois átomos do mesmo elemento.
Alguns exemplos de elementos diatômicos são o oxigênio (O2), o nitrogênio (N2) e o hidrogênio (H2). Estas moléculas são formadas por dois átomos ligados entre si, compartilhando elétrons de forma estável.
Os elementos diatômicos desempenham um papel fundamental em diversos processos naturais, como a respiração celular, a formação de proteínas e a composição da atmosfera terrestre. Além disso, muitos desses compostos são essenciais para a vida como a conhecemos.
Portanto, os elementos diatômicos são uma importante categoria de moléculas que contribuem para a diversidade e complexidade da química presente na natureza.
Quais são os componentes essenciais da química?
Na química, os componentes essenciais são os elementos químicos, que são substâncias puras compostas por átomos do mesmo tipo. Os elementos químicos são representados por símbolos químicos, e podem se combinar para formar compostos químicos. Um exemplo de elementos essenciais são os elementos diatômicos, que são compostos por dois átomos da mesma espécie ligados entre si.
Os elementos diatômicos são moléculas formadas por dois átomos do mesmo elemento químico. Alguns exemplos de elementos diatômicos são oxigênio (O2), nitrogênio (N2) e cloro (Cl2). Esses elementos diatômicos são muito importantes na química, pois estão presentes em diversos processos químicos e reações.
Em resumo, os elementos diatômicos são componentes essenciais da química, pois são moléculas formadas por dois átomos do mesmo elemento químico que desempenham um papel fundamental em diversas reações químicas.
Do que são compostas as moléculas?
As moléculas são compostas por elementos químicos que se unem por meio de ligações químicas. Os elementos diatômicos são um tipo específico de moléculas que são compostas por dois átomos do mesmo elemento. Eles são formados por elementos que naturalmente se ligam em pares, como o oxigênio (O2), o hidrogênio (H2), o nitrogênio (N2) e o flúor (F2).
Esses elementos diatômicos são chamados assim porque são formados por dois átomos ligados entre si. Eles podem se unir dessa forma por meio de ligações covalentes, compartilhando elétrons para alcançar estabilidade. Essas moléculas diatômicas são fundamentais em diversos processos químicos e estão presentes em muitas substâncias do nosso cotidiano.
Portanto, as moléculas são compostas por elementos químicos que se unem por meio de ligações químicas, e os elementos diatômicos são um exemplo disso, formados por dois átomos do mesmo elemento que se ligam naturalmente em pares. Eles desempenham um papel importante em diversas reações químicas e são essenciais para a formação de diferentes substâncias.
Quais são os elementos diatômicos?
Os elementos diatómicas , também chamados homonuclear moléculas diatómicas são compostos de apenas dois átomos dos mesmos elementos químicos (Helmenstine, 2017).
Alguns elementos não podem existir por si mesmos, mesmo quando isolados de qualquer outro tipo de átomo. Elementos desta natureza serão combinados com átomos do mesmo elemento para serem estáveis.

Em outras palavras, o hidrogênio, um elemento diatômico, não pode ser por si só. Não pode simplesmente haver H.
O hidrogênio é tão reativo que quando todo, exceto o hidrogênio, é isolado, ele é combinado em uma molécula diatômica (de dois átomos).
Portanto, o gás hidrogênio, que às vezes é usado como combustível, existe como H 2 (Diatomic Elements, SF).
Moléculas diatômicas
As moléculas diatômicas contêm dois átomos quimicamente ligados. Se os dois átomos são idênticos, como a molécula de oxigênio (O 2 ), forma uma molécula diatômica homonuclear, enquanto que se os átomos são diferentes, como na molécula de monóxido de carbono (CO), forma uma molécula diatômica heteronuclear
As moléculas contendo mais do que duas moléculas de poliatómicos são chamados de átomos, por exemplo, dióxido de carbono (CO 2 ) e ua (H 2 O). As moléculas de polímero podem conter muitos milhares de átomos componentes (Encyclopædia Britannica, 2016).
Existem sete elementos que formam moléculas diatômicas. Os seguintes 5 gases dos elementos são encontrados como moléculas diatômicas à temperatura e pressão ambiente:
-Hidrogênio – H 2
-Nitrogênio – N 2
-Oxigênio – O 2
-Fluoreto – F 2
-Cloro – Cl 2
O bromo e o iodo geralmente existem na forma líquida, mas também como gases diatômicos a temperaturas ligeiramente mais altas, perfazendo um total de 7 elementos diatômicos.
-Bromo – Br 2
-Iodo – I 2
Os elementos diatômicos são halogênios (flúor, cloro, bromo, iodo) e elementos com uma terminação – hidrogênio (hidrogênio, oxigênio, nitrogênio). A astatina é outro halogênio, mas seu comportamento é desconhecido (Helmenstine A., 2014).
Propriedades dos elementos diatômicos
Todas as moléculas diatômicas são lineares, que é o arranjo espacial mais simples de átomos.
É conveniente e comum representar uma molécula diatômica como duas massas pontuais (os dois átomos) conectadas por uma mola sem massa.
As energias envolvidas nos movimentos da molécula podem ser divididas em três categorias:
- Energias translacionais (a molécula que se move do ponto A ao ponto B)
- As energias de rotação (a molécula girando em torno de seu eixo)
- Energias vibratórias (moléculas que vibram de várias maneiras)
Todos os elementos diatômicos são gases à temperatura ambiente, com exceção do bromo e do iodo, que são líquidos (o iodo pode estar no estado sólido) e todos os elementos diatômicos, com exceção do oxigênio e do nitrogênio, são unidos por uma ligação simples.
A molécula de oxigênio tem seus dois átomos ligados por uma ligação dupla e a do nitrogênio por uma ligação tripla (Boundless, SF).
Alguns elementos diatômicos
Hidrogênio
Hidrogênio (H 2 ), com um número atómico de 1, é um gás incolor que não foi formalmente descoberto como um elemento por Henry Cavendish para 1766, mas foi acidentalmente encontrado cerca de cem anos atrás por Robert Boyle.
É um gás incolor, inodoro e não tóxico que existe naturalmente em nosso Universo. Sendo o primeiro elemento da tabela periódica, o hidrogênio é o mais leve e mais abundante de todos os elementos químicos do universo, uma vez que compõe 75% de sua massa.
Nitrogênio
O nitrogênio (N 2 ) tem um número atômico de sete e constitui aproximadamente 78,05% da atmosfera da Terra em volume.
É um gás inodoro, incolor e principalmente inerte, e permanece incolor e inodoro no estado líquido.
Oxigênio
O oxigênio (O 2 ) tem um número atômico de oito. Esse gás incolor e inodoro possui oito prótons no núcleo e é azul pálido em seus estados líquido e sólido.
Um quinto da atmosfera da Terra é composto de oxigênio e é o terceiro elemento mais abundante no universo de massas.
O oxigênio é o elemento mais abundante em massa na biosfera da Terra. A alta concentração de oxigênio na atmosfera é o resultado do ciclo de oxigênio da Terra, que é predominantemente impulsionado pela fotossíntese das plantas (Oxygen Facts, SF).
Flúor
O flúor (F 2 ) possui um número atômico de nove e é o mais reativo e eletronegativo de todos os elementos. Este elemento não metálico é um gás amarelo pálido que é um membro do grupo halogênio.
Aparentemente, George Gore foi o primeiro cientista a isolar o flúor, mas seu experimento explodiu quando o flúor produzido reagiu com o hidrogênio.
Em 1906, Ferdinand Frederic Henri Moissan recebeu o Prêmio Nobel de Química por seu trabalho em isolamento de fluoreto em 1886. É o elemento mais eletronegativo da tabela periódica.
Cloro
O cloro (Cl 2 ) é um membro do grupo halogênio com um número atômico de dezessete. Uma de suas formas, NaCl, está em uso desde os tempos antigos.
O cloro está em uso há milhares de anos de muitas outras maneiras, mas não foi nomeado até 1810 por Sir Humphry Davy.
O cloro na sua forma pura é verde amarelado, mas seus compostos comuns são geralmente incolores (Chlorine Facts, SF).
Bromo
O bromo (Br 2 ) tem um número atômico de trinta e cinco. É um líquido marrom escuro pesado, o único elemento não metálico que é um líquido.
O bromo foi descoberto por Antoine J. Balard em 1826. Foi usado para fins importantes muito antes de ser formalmente descoberto.
Iodo
O iodo (I 2 ) tem um número atômico de cinquenta e três, com cinquenta e três prótons no núcleo de um átomo. É um não metal azul-preto que desempenha um papel muito importante na química orgânica.
O iodo foi descoberto em 1811 por Barnard Courtois. Ele o nomeou iodo da palavra grega “iodes”, que significa violeta. É um sólido azul-preto.
O iodo desempenha um papel muito importante na biologia de todos os organismos vivos, pois sua deficiência leva a doenças como hipertireoidismo e hipotireoidismo (Royal Society of Chemistry, 2015).
Referências
- (SF). Moléculas Diatômicas Homonucleares . Recuperado de boundless.com.
- Cloro factos . (SF). Recuperado de softschools.com.
- Elementos diatómicas . (SF). Recuperado de ths.talawanda.org.
- Encyclopædia Britannica. (14 de setembro de 2016). Molécula . Recuperado de britannica.com.
- Helmenstine, A. (2014, 28 de setembro). Elementos diatómicas . Recuperado de sciencenotes.org.
- Helmenstine, AM (2017, 29 de março). Quais são os sete elementos diatômicos? Recuperado de thoughtco.com.
- Oxigênio factos . (SF). Recuperado de softschools.com.
- Sociedade Real de Química. (2015). iodo molecular . Recuperado de chemspider.com.