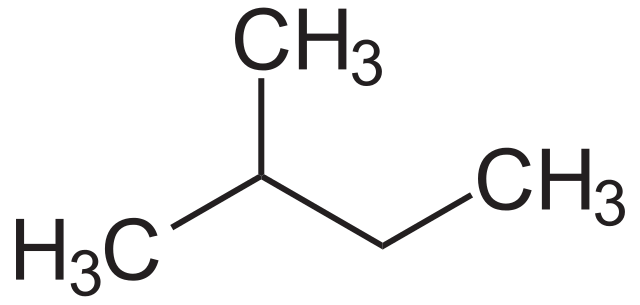
O isopentano, também conhecido como 2-metilbutano, é um hidrocarboneto saturado de cadeia ramificada com fórmula química C5H12. Possui uma estrutura molecular em forma de ramificação, o que lhe confere propriedades físicas e químicas únicas. Suas principais propriedades incluem baixo ponto de ebulição, alta volatilidade e odor característico. O isopentano é amplamente utilizado como solvente em indústrias químicas e farmacêuticas, além de ser empregado na produção de polímeros, combustíveis e aerossois. Sua produção é realizada através da destilação fracionada do petróleo ou da craqueamento de hidrocarbonetos mais pesados.
Qual é a utilidade do Isopentano em processos químicos e industriais?
O Isopentano, também conhecido como metilbutano, é um hidrocarboneto saturado de cinco carbonos e apresenta a fórmula molecular C5H12. Sua estrutura é composta por uma cadeia ramificada com um grupo metil ligado a um carbono secundário. Este composto possui propriedades físicas que o tornam extremamente útil em diversos processos químicos e industriais.
Uma das principais propriedades do Isopentano é o seu baixo ponto de ebulição, que é de aproximadamente -11°C. Isso significa que ele é volátil e se evapora rapidamente em condições normais de pressão e temperatura. Essa característica faz com que o Isopentano seja amplamente utilizado como solvente em processos de extração e purificação de compostos orgânicos.
Além disso, o Isopentano também é empregado como agente refrigerante em sistemas de refrigeração devido à sua capacidade de absorver calor rapidamente e evaporar a baixas temperaturas. Sua eficiência como refrigerante o torna uma escolha comum em aplicações industriais, como em sistemas de refrigeração de laboratórios e em processos de criogenia.
Na indústria química, o Isopentano é utilizado na produção de diversos compostos, como plásticos, resinas e borrachas sintéticas. Sua capacidade de atuar como agente de expansão em polímeros o torna essencial na fabricação de materiais isolantes e espumantes.
A produção de Isopentano é realizada principalmente através da destilação fracionada de frações de petróleo ou da craqueamento de hidrocarbonetos de cadeia longa. Após o processo de purificação, o Isopentano está pronto para ser utilizado em uma variedade de aplicações industriais e químicas.
Sua versatilidade o torna um componente essencial em diversas áreas da indústria moderna.
Usos e aplicações do pentano na indústria e química.
O pentano é um hidrocarboneto saturado pertencente à classe dos alcanos, com fórmula molecular C5H12. Ele é um líquido incolor e inflamável, com um odor característico. O pentano é amplamente utilizado na indústria e química devido às suas propriedades e características.
Na indústria, o pentano é utilizado como solvente em várias aplicações, tais como na fabricação de poliestireno expandido (isopor), na extração de óleos vegetais e na produção de tintas e vernizes. Além disso, é empregado como propelente em aerossóis e como refrigerante em sistemas de refrigeração.
Na química, o pentano é utilizado como padrão em análises cromatográficas e espectrométricas, devido à sua pureza e baixa toxicidade. Também é utilizado como matéria-prima na síntese de outros compostos orgânicos.
A produção de pentano é realizada principalmente por meio da destilação fracionada do petróleo bruto, onde é separado juntamente com outros hidrocarbonetos de cadeia linear. Outro método de produção é a partir da craqueamento de hidrocarbonetos de cadeia mais longa.
Isopentano: estrutura, propriedades, usos, produção

O isopentano é um composto orgânico que é condensado fórmula (CH 3 ) 2 CHCH 2 CH 3 . É um alcano, especificamente um isômero ramificado de pentano, caracterizado por ser um líquido altamente volátil e usado como agente espumante. Atualmente, seu nome mais recomendado pela IUPAC é 2-metilbutano.
Na imagem abaixo, sua fórmula estrutural pode ser vista. Note-se que um CH 3 grupo é efectivamente ligado ao carbono 2 da cadeia butilo. A partir do isopentano é obtido o substituinte ou radical isopentil ou isopentil, sendo um dos substituintes alquílicos mais volumosos que possam existir.
O isopentano é um composto apolar, hidrofóbico e inflamável. Seu cheiro é semelhante ao da gasolina e faz parte de sua composição, pois aumenta seu número de octanas ou octanas. É obtido a partir da reação de isomerização do n- pentano, embora naturalmente seja obtido em pequenas quantidades nas reservas de gás natural.
À parte seu caráter altamente inflamável, o isopentano é considerado uma substância não tóxica. Pode ser ingerido e perfumado com moderação por uma pessoa antes que ocorram sintomas indesejáveis, como vômitos e tonturas. O isopentano pode ser encontrado em cremes de barbear e condicionadores de cabelo.
Estrutura de isopentano
Na imagem superior, temos a estrutura molecular do isopentano, representada por um modelo de esferas e barras. As esferas pretas correspondem aos átomos de carbono, enquanto as esferas brancas correspondem aos átomos de hidrogênio. Pode-se dizer que seu esqueleto de carbono é robusto, ramificado e volumoso.
As extremidades da molécula de isopentano são compostos de CH 3 grupos , que são ineficientes quando se trata de reforçar as interacções intermoleculares. As moléculas de isopentano dependem das forças dispersivas de Londres e de suas massas para poder permanecer coesas e, assim, definir um líquido sob condições normais de temperatura e pressão.
Entretanto, sua geometria e os grupos CH 3 são responsáveis pelo líquido isopentano ser altamente volátil e ferver a uma temperatura de 28,2 ºC. Por exemplo, o isômero linear de n- pentano ferve em torno de 36 ºC, refletindo suas melhores interações intermoleculares.
Apesar de sua aparente robustez, a molécula de isopentano é capaz de assumir várias configurações espaciais, fator essencial para estabelecer seu cristal a uma temperatura de -160 ºC.
Propriedades
Aparência física
Líquido ou gás incolor, com aparência aquosa e que também exala um odor semelhante à gasolina. É uma substância altamente volátil.
Ponto de fusão
O isopentano cristaliza em uma faixa de temperatura entre -161 e -159 ºC.
Ponto de ebulição
O isopentano ferve a uma temperatura entre 27,8 e 28,2 ºC. Portanto, assim que for exposto fora de seu recipiente, começará a ferver e liberar grandes volumes de vapor.
Pressão de vapor
76,9 kPa a 20 ºC (cerca de 0,76 atm)
Densidade
0,6201 g / mL a 20 ºC. Os vapores de isopentano são 2,48 mais densos que o ar.
Solubilidade
O isopentano, sendo uma substância apolar, é insolúvel e imiscível com água e alguns álcoois. É solúvel e miscível em solventes parafínicos, éteres, tetracloreto de carbono e também em líquidos aromáticos, como o tolueno.
Índice de refração
1.354
Tensão superficial
15 dyn / cm a 20 ºC
Viscosidade
0,214 cP a 20 ºC
Ponto de inflamação
-51 ºC. Essa temperatura converte o isopentano em uma substância perigosamente inflamável; portanto, seus produtos devem ser mantidos o mais longe possível de qualquer fonte de chama ou calor.
Temperatura de auto-ignição
420 ºC
Formulários
O isopentano é um solvente orgânico que serve como meio de reação para certas sínteses orgânicas e também representa a matéria- prima para a produção de outros compostos.
É adicionado à gasolina para aumentar seu número de octanas e a vários produtos cosméticos para melhorar sua textura, como cremes de barbear, uma vez que evapora rapidamente e deixa para trás uma massa borbulhante.
Da mesma forma, o poliestireno é umedecido em isopentano, para que, quando evapore, expanda o plástico até criar uma espécie de espuma, com a qual são projetados óculos, modelos, pratos, bandejas etc.
Por outro lado, na criogenia o isopentano é usado, juntamente com gelo seco e nitrogênio líquido, para congelar tecidos e amostras biológicas.
Obtenção
O isopentano pode ser obtido em reservatórios de gás natural, mas ocupa apenas 1% de seu conteúdo.
Outra rota, a mais utilizada no nível industrial, começa a partir do n- pentano destilado dos processos de refino de petróleo. Então o n- pentano passa por uma reação especial chamada isomerização .
O objetivo da isomerização do n- pentano é obter seus isômeros mais ramificados. Assim, entre os produtos, temos não apenas o isopentano, mas também o neopentano. Essa reação é possível através do uso de catalisadores metálicos muito específicos, que controlam qual temperatura e quais pressões são necessárias.
Riscos
O isopentano é considerado uma substância não tóxica. Isso se deve em parte à sua baixa reatividade, uma vez que suas ligações CC ou CH não são fáceis de quebrar, portanto não interferem como tal em nenhum processo metabólico. De fato, uma pessoa é capaz de inalar grandes quantidades de seus vapores antes de sofrer asfixia, sem aparentemente sofrer danos colaterais.
Sua ingestão causa náuseas e vômitos, e seu contato com a pele acaba secando-a. Por outro lado, estudos médicos não foram capazes de determinar se o isopentano é uma substância cancerígena. No entanto, é considerado um poluente perigoso para os ecossistemas marinhos e sua fauna.
O maior perigo em torno do isopentano não é tanto sua reatividade, mas sua inflamabilidade: queima com o oxigênio no ar. E como seu líquido é altamente volátil, o menor vazamento libera muitos de seus vapores no ambiente, que se inflamam na proximidade mais próxima de uma chama ou qualquer outra fonte de calor.
É por isso que os produtos que contêm isopentano devem ser armazenados em ambientes seguros e frescos.
Referências
- Graham Solomons TW, Craig B. Fryhle. (2011). Química Orgânica . (10 ª edição). Wiley Plus.
- Carey F. (2008). Química Orgânica . (Sexta edição). Mc Graw Hill.
- Morrison e Boyd. (1987). Química orgânica . (Quinta edição). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Isopentano. Recuperado de: en.wikipedia.org
- Centro Nacional de Informação Biotecnológica. (2020). Isopentano. Banco de Dados PubChem. CID = 6556. Recuperado de: pubchem.ncbi.nlm.nih.gov
- Elsevier BV (2020). Isopentano. ScienceDirect. Recuperado de: sciencedirect.com
- Jennifer B. Galvin e Fred Marashi. (2010). 2-metilbutano (isopentano). Jornal de Toxicologia e Saúde Ambiental, Parte A Atual Issues. Volume 58, 1999 – Edição 1-2. doi.org/10.1080/009841099157403