A separabilidade química é o processo de separar diferentes substâncias presentes em uma mistura com base em suas propriedades químicas. Neste processo, as substâncias são separadas de acordo com suas características específicas, como solubilidade, densidade, ponto de ebulição, entre outros. Este método é amplamente utilizado em laboratórios e indústrias para purificar e isolar substâncias, bem como para identificar e quantificar componentes de uma amostra. Neste artigo, exploraremos os conceitos e exemplos de separabilidade química, destacando sua importância e aplicações práticas.
Introdução à Química: Fundamentos e Conceitos Essenciais em formato pdf.
Introdução à Química: Fundamentos e Conceitos Essenciais em formato pdf é um material fundamental para quem deseja compreender os princípios básicos dessa ciência. Neste documento, são abordados os conceitos fundamentais da química, desde a estrutura do átomo até as reações químicas.
Este material é essencial para estudantes que estão iniciando seus estudos em química, pois fornece uma base sólida para o entendimento de fenômenos químicos. Além disso, o formato pdf permite que o conteúdo seja facilmente acessado e compartilhado.
Com a leitura deste material, os leitores poderão adquirir os conhecimentos necessários para compreender os fundamentos da química e aplicá-los em diferentes contextos. Portanto, é altamente recomendado para quem deseja aprofundar seus conhecimentos nessa área.
Portanto, baixe agora mesmo o Introdução à Química: Fundamentos e Conceitos Essenciais em formato pdf e dê o primeiro passo para conhecer os princípios básicos dessa ciência fascinante.
Separabilidade química: conceitos e exemplos
A separabilidade química é um processo fundamental na química que permite a separação de diferentes substâncias com base em suas propriedades químicas. Esse processo é essencial em diversas áreas, como na indústria química e na pesquisa científica.
Existem diferentes métodos de separabilidade química, como a destilação, a extração e a filtração. Cada método é utilizado de acordo com as propriedades das substâncias a serem separadas, garantindo a eficiência do processo.
Um exemplo comum de separabilidade química é a destilação simples, que é utilizada para separar líquidos miscíveis com diferentes pontos de ebulição. Nesse processo, a mistura é aquecida até que um dos componentes atinja seu ponto de ebulição, vaporizando e sendo condensado em outro recipiente.
Portanto, a separabilidade química é um conceito fundamental na química que permite a separação de substâncias com base em suas propriedades químicas, sendo essencial para diversas aplicações práticas.
Exemplos de matéria, corpo e objeto: entenda as diferenças e características de cada um.
A separabilidade química é um conceito fundamental para entender a composição e as propriedades da matéria. Para compreender melhor esse conceito, é importante diferenciar as noções de matéria, corpo e objeto.
A matéria é tudo o que ocupa lugar no espaço e possui massa. Ela pode se apresentar de diversas formas, como sólidos, líquidos e gases. Um exemplo de matéria é a água, que pode ser encontrada no estado líquido, sólido (gelo) ou gasoso (vapor). A matéria é o elemento básico que constitui todos os corpos e objetos do universo.
Um corpo é uma porção delimitada de matéria que possui uma forma e tamanho específicos. Por exemplo, uma cadeira, uma mesa e um carro são exemplos de corpos, pois possuem uma estrutura definida e ocupam um espaço no ambiente. Os corpos são compostos por diferentes tipos de matéria, que se organizam de acordo com suas propriedades físicas e químicas.
Já um objeto é um corpo ou conjunto de corpos que tem uma função ou finalidade específica. Por exemplo, um celular, um livro ou um avião são exemplos de objetos, pois foram projetados para cumprir determinadas tarefas ou satisfazer necessidades humanas. Os objetos podem ser compostos por uma variedade de materiais e substâncias, que se combinam de maneira a atender às exigências de seu uso.
Portanto, ao entender as diferenças entre matéria, corpo e objeto, é possível compreender melhor a composição e a estrutura dos elementos que nos cercam. A separabilidade química se baseia na capacidade de identificar e separar os componentes de uma substância ou mistura, a fim de estudar suas propriedades e comportamentos. Através desse processo, é possível analisar as relações entre os diferentes elementos químicos e compreender como eles interagem entre si.
Principais fundamentos da química em 15 palavras: conceitos essenciais para compreender a ciência dos elementos.
Os principais fundamentos da química incluem átomos, moléculas, reações químicas, energia, estrutura, propriedades e compostos.
A separabilidade química é a capacidade de separar diferentes substâncias com base em suas propriedades.
Exemplos de separabilidade química incluem destilação, filtração, extração e cromatografia como métodos de separação.
Compreender os conceitos fundamentais da química é essencial para entender a natureza dos elementos e compostos.
Portanto, estudar a separabilidade química é crucial para identificar e purificar substâncias em laboratório.
Resumo simplificado dos conceitos fundamentais da Química em poucas palavras.
A Química é a ciência que estuda a composição, estrutura, propriedades e transformações da matéria. Ela se baseia em alguns conceitos fundamentais, como átomos, moléculas, elementos químicos, compostos químicos, reações químicas e energia. A separabilidade química é um processo que permite separar diferentes substâncias em uma mistura com base em suas propriedades químicas. Alguns métodos de separação química incluem a destilação, filtração, cristalização, extração e cromatografia. Esses métodos são essenciais para a indústria química, laboratórios de pesquisa e diversas aplicações práticas.
Separabilidade química: conceitos e exemplos
Podemos definir divisibilidade na química como uma propriedade da matéria que permite que ela se separe em porções menores (Miller, 1867).
Para entender o conceito, podemos dar um exemplo. Se pegarmos um pedaço de pão e cortá-lo ao meio repetidas vezes, chegaremos a um bloco fundamental de matéria que não pode ser dividido mais? Esta questão está presente na mente de cientistas e filósofos há milhares de anos.
Origem e conceito de divisibilidade química
Durante muito tempo, foi debatido se a matéria era composta de partículas (o que hoje conhecemos como átomos); no entanto, a ideia geral era que a matéria fosse um continuum que pudesse ser dividido.
Esse conceito generalizado fez de cientistas brilhantes como James Clerk Maxwell (das equações de Maxwell ) e Ludwing Boltzman (da distribuição Boltzman) uma zombaria, que arrastou os primeiros à loucura e os segundos ao suicídio.
No século V aC, o filósofo grego Leucipo e seu discípulo Demócrito usaram a palavra átomos para designar o menor pedaço individual de matéria e propuseram que o mundo consistisse apenas de átomos em movimento.
Essa teoria atômica inicial diferia das versões posteriores, pois incluía a idéia de uma alma humana composta por um tipo de átomo mais refinado distribuído por todo o corpo.
A teoria atômica caiu em declínio na Idade Média, mas reviveu no início da revolução científica no século XVII.
Isaac Newton , por exemplo, acreditava que a matéria consistia em “partículas sólidas, massivas, duras, impenetráveis e móveis”.
A divisibilidade pode ser dada por diferentes métodos, o mais comum é a divisibilidade por métodos físicos, por exemplo, pique uma maçã com uma faca.
No entanto, a divisibilidade também pode ser dada por métodos químicos, onde a matéria seria separada em moléculas ou átomos.
10 exemplos de divisibilidade química
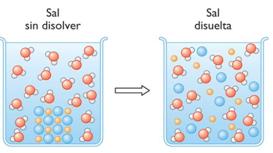
1- Dissolver sal em água
Quando um sal é dissolvido, por exemplo cloreto de sódio na água, ocorre um fenômeno de solvatação onde as ligações iônicas do sal são quebradas:
NaCl → Na + + Cl –
Ao dissolver apenas um grão de sal na água, ele se separará em bilhões de íons de sódio e cloreto em solução.
2- Oxidação de metais em meio ácido
Todos os metais, por exemplo magnésio ou zinco, reagem com ácidos, por exemplo, ácido clorídrico diluído para produzir bolhas de hidrogênio e uma solução incolor do cloreto de metal.
Mg + HCl → Mg 2+ + Cl – + H 2
O ácido oxida o metal separando as ligações metálicas para obter íons em solução (BBC, 2014).
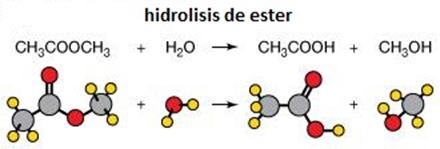
3- Hidrólise do éster
Hidrólise é a quebra de uma ligação química através da água. Um exemplo de hidrólise é a hidrólise de ésteres, onde eles são divididos em duas moléculas, um álcool e um ácido carboxílico (Clark, 2016).
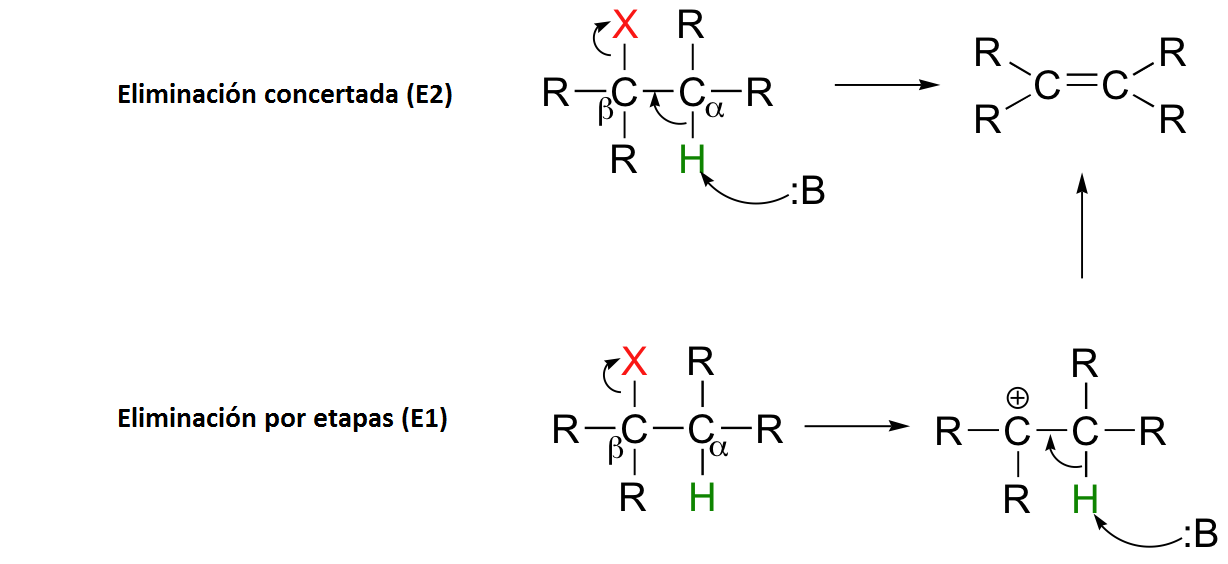
4- Reacções de eliminação
Uma reação de eliminação faz exatamente o que diz: elimina os átomos de uma molécula. Isso é feito para criar uma ligação dupla carbono-carbono. Isso pode ser feito usando uma base ou um ácido (Foist, SF).
Pode ocorrer em uma única etapa combinada (a abstração de prótons em Cα que ocorre ao mesmo tempo que a clivagem da ligação Cβ-X) ou em duas etapas (a clivagem da ligação Cβ-X ocorre primeiro para formar um carbococo intermediário, que é então “desligado” pela abstração do próton no carbono alfa) (Soderberg, 2016).
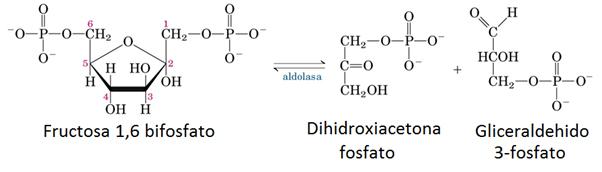
5- Reação enzimática da aldolase
Na fase preparatória da glicólise, uma molécula de glicose é dividida em duas moléculas de gliceraldeído 3-fosfato (G3P) usando 2 ATP.
A enzima responsável por esta incisão é a aldolase, que através de uma condensação reversa divide a molécula de 1,6-bifosfato de frutose em duas em uma molécula G3P e uma molécula de fosfato de di-hidroxiacetona que é subsequentemente isomerizada para formar outra molécula de G3P
6- Degradação de biomoléculas
Não apenas a glicólise, mas toda a degradação de biomoléculas nas reações de catabolismo são exemplos de divisibilidade química.
Isso ocorre porque eles partem de grandes moléculas, como carboidratos, ácidos graxos e proteínas, para produzir moléculas menores, como acetil-CoA, que entra no ciclo de Krebs para produzir energia na forma de ATP.
7- Reacções de combustão
Este é um outro exemplo de divisibilidade química desde moléculas complexas como propano ou butano reagir com o oxigénio para produzir CO 2 e água:
C 3 H 8 + 5 O 2 → 3CO 2 + 4H 2 O
Pode-se dizer que a degradação das biomoléculas é uma reação de combustão, uma vez que os produtos finais são CO 2 e água, porém estes são dados em várias etapas com diferentes intermediários.
8- Centrifugação do sangue
A separação dos diferentes componentes do sangue é um exemplo de divisibilidade. Apesar de ser um processo físico, acho o exemplo interessante, pois os componentes são separados por centrifugação por diferença de densidade.
Os componentes mais densos, o soro com os glóbulos vermelhos , permanecerão no fundo do tubo de centrifugação, enquanto os menos densos, o plasma, permanecerão no topo.
9- Tampão de bicarbonato
bicarbonato de sódio, HCO 3 – , é a forma principal para transportar CO 2 no produto do corpo reacções de degradação metabólica.
Este composto reage com um próton do meio para produzir ácido carbônico que é subsequentemente dividido em CO2 e água:
HCO 3 – + H + DH 2 CO 3 D CO 2 + H 2 O
Como as reações são reversíveis, é assim que o corpo, através da respiração, controla o pH fisiológico para evitar processos de alcalose ou acidose.
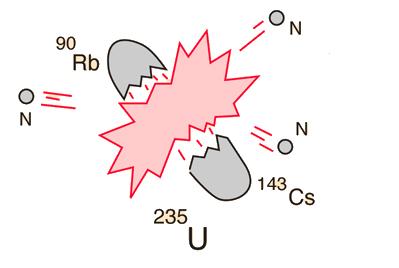
10- Divisão do átomo ou fissão nuclear
Caso um núcleo maciço (como o urânio-235) seja quebrado (fissões), resultará em um rendimento líquido de energia.
Isso ocorre porque a soma das massas dos fragmentos será menor que a massa do núcleo de urânio (Fissão Nuclear, SF).
No caso de a massa dos fragmentos ser igual ou maior que a do ferro no pico da curva de energia de ligação, as partículas nucleares serão mais fortemente ligadas do que no núcleo de urânio e essa diminuição na massa ocorrerá em a forma de energia de acordo com a equação de Einstein.
Para elementos mais leves que o ferro, a fusão produzirá energia. Este conceito levou à criação da bomba atômica e energia nuclear (AJ Software & Multimedia, 2015).
Referências
- AJ Software e Multimídia. (2015). Fissão Nuclear: Fundamentos. Recuperado de atomicarchive.com.
- (2014). Reações de ácidos. Recuperado de bbc.co.uk.
- Clark, J. (2016, janeiro). HIDROLISANDO ÉSTERES. Recuperado de chemguide.co.uk.
- Foist, L. (SF). Reações de eliminação na química orgânica. Recuperado de study.com.
- Miller, WA (1867). Elementos de Química: Teórico e Prático, Parte 1. Nova York: John Wiley e filho.
- Fissão Nuclear (SF). Recuperado da hiperfísica.
- Pratt, D. (1997, novembro). A Divisibilidade Infinita da Matéria. Recuperado de davidpratt.info.
- Soderberg, T. (2016, 31 de maio). Eliminação pelos mecanismos E1 e E2. Recuperado de chem.libretext.