O ácido tartárico é um composto orgânico encontrado naturalmente em várias frutas, como uvas, bananas e tâmaras. Sua estrutura química é composta por dois grupos carboxílicos e dois grupos hidroxila, o que confere propriedades ácidas e de ligação de hidrogênio ao composto. O ácido tartárico é amplamente utilizado na indústria alimentícia, farmacêutica e química, devido às suas propriedades como acidulante, estabilizante e agente redutor. Neste artigo, exploraremos a estrutura molecular, aplicações e propriedades do ácido tartárico em diferentes contextos.
Para que serve o ácido tartárico e qual sua importância na indústria alimentícia?
O ácido tartárico é um composto orgânico encontrado naturalmente em diversas frutas, como uvas e bananas. Ele é amplamente utilizado na indústria alimentícia como aditivo por sua capacidade de realçar o sabor e preservar a cor dos alimentos. Além disso, o ácido tartárico também é utilizado como estabilizante em produtos como refrigerantes, gelatinas e sorvetes.
Na indústria alimentícia, o ácido tartárico desempenha um papel fundamental na produção de vinhos, uma vez que auxilia na fermentação do mosto da uva. Além disso, ele também é utilizado na fabricação de produtos de confeitaria, como bolos e biscoitos, onde atua como agente levedante.
Além de sua importância na indústria alimentícia, o ácido tartárico também possui diversas aplicações em outros setores, como na indústria farmacêutica e na produção de produtos de limpeza. Sua versatilidade e propriedades únicas o tornam um composto indispensável em diversos processos industriais.
Descubra as propriedades do ácido tartárico e sua utilidade na culinária e na indústria.
O ácido tartárico é um composto orgânico encontrado naturalmente em frutas como uvas e tâmaras. Sua estrutura química consiste em dois grupos carboxílicos e um grupo hidroxila, o que confere a ele propriedades ácidas e solúveis em água.
Na culinária, o ácido tartárico é amplamente utilizado como um aditivo alimentar, especialmente na fabricação de vinhos. Ele é adicionado durante o processo de fermentação para ajudar a equilibrar o sabor e a acidez da bebida. Além disso, o ácido tartárico é utilizado na fabricação de doces, geléias e refrigerantes, onde atua como estabilizante e acidulante.
Na indústria, o ácido tartárico é utilizado em diversos processos, como na fabricação de produtos farmacêuticos, cosméticos e produtos químicos. Ele também é empregado na indústria de materiais de construção, na produção de tintas e vernizes, e como um agente de limpeza e polimento.
Além de suas aplicações na culinária e na indústria, o ácido tartárico possui propriedades únicas que o tornam um composto versátil e indispensável em diversos setores. Sua capacidade de formar complexos com metais, por exemplo, é amplamente explorada em processos de purificação e separação de substâncias.
Onde é possível localizar o ácido tartárico para uso industrial e culinário?
O ácido tartárico é uma substância natural encontrada em diversas fontes, sendo mais comumente extraído de uvas e de outras frutas ácidas, como o tamarindo e o limão. Além disso, o ácido tartárico também pode ser produzido sinteticamente em laboratório para uso industrial e culinário.
Na indústria alimentícia, o ácido tartárico é utilizado como um aditivo para conferir acidez e sabor a diversos produtos, como refrigerantes, doces, geléias e vinhos. Já na indústria química, o ácido tartárico é empregado em processos de síntese de compostos químicos e na fabricação de produtos farmacêuticos.
Portanto, tanto para uso industrial quanto culinário, o ácido tartárico pode ser obtido a partir de fontes naturais, como uvas e frutas ácidas, ou produzido sinteticamente em laboratório.
Descubra qual fruta possui o ácido tartárico em sua composição natural.
O ácido tartárico é um ácido orgânico presente em diversas frutas, sendo mais comum em uvas. Este ácido é responsável pelo sabor característico e pela acidez das uvas, sendo também utilizado na produção de vinhos para controlar a acidez da bebida.
O ácido tartárico possui uma estrutura molecular simples, formada por duas moléculas de ácido málico, o que confere a ele propriedades únicas. Além de ser utilizado na indústria de alimentos, o ácido tartárico também é empregado na indústria farmacêutica e na produção de produtos de limpeza.
Suas propriedades ácidas fazem do ácido tartárico um ingrediente versátil, podendo ser utilizado como acidulante, estabilizante e antioxidante. Além disso, este ácido também é utilizado na fabricação de produtos cosméticos, como cremes e loções, devido às suas propriedades benéficas para a pele.
Em resumo, o ácido tartárico é um composto químico presente em diversas frutas, sendo mais comum em uvas. Suas propriedades e aplicações são diversas, tornando-o um ingrediente essencial em diversos setores industriais.
Ácido Tartárico: Estrutura, Aplicações e Propriedades
O ácido tartárico é um composto orgânico, cuja fórmula molecular é COOH (CHOH) 2 COOH. Possui dois grupos carboxila; isto é, ele pode liberar dois prótons (H + ). Em outras palavras, é um ácido diprótico. Também pode ser classificado como um ácido aldárico (açúcar ácido) e um derivado do ácido succínico.
Seu sal é conhecido desde tempos imemoriais e é um dos produtos secundários da vinificação. Cristaliza como sedimento branco batizado como “diamante de vinho”, que se acumula na cortiça ou no fundo dos barris e garrafas. Este sal é bitartarato de potássio (ou tartarato de ácido potássico).

Os sais do ácido tartárico têm em comum a presença de um ou dois cátions (Na + , K + . NH 4 + , Ca 2+ , etc.) porque, quando liberam seus dois prótons, permanecem carregados negativamente com uma carga de -1 (como com sais de bitartarato) ou -2.
Por sua vez, esse composto tem sido objeto de estudo e ensino de teorias orgânicas relacionadas à atividade óptica, mais precisamente com a estereoquímica.
Onde está?
O ácido tartárico é um componente de muitas plantas e alimentos, como damascos, abacates, maçãs, tamarindos, sementes de girassol e uvas.
No processo de envelhecimento do vinho, esse ácido – a baixas temperaturas – é combinado com potássio para cristalizar como tartarato. Nos vinhos tintos, a concentração desses tartaratos é menor, enquanto nos vinhos brancos eles são mais abundantes.
Tartaratos são sais de cristais brancos, mas quando obstruem as impurezas do ambiente alcoólico, adquirem tons avermelhados ou roxos.
Estrutura
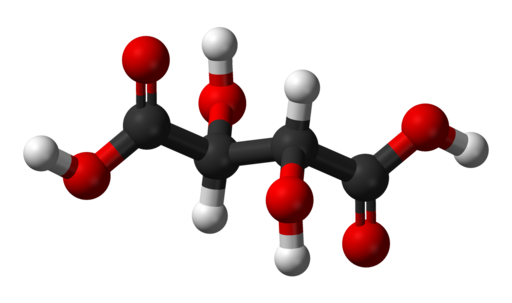
A estrutura molecular do ácido tartárico é representada na imagem superior. Os grupos carboxi (-COOH) estão localizados nas extremidades laterais e são separados por uma cadeia curta de dois carbonos (C 2 e C 3 ).
Por sua vez, cada um desses carbonos está ligado a um grupo H (esfera branca) e um grupo OH. Esta estrutura pode rodar o C 2 -C 3 , gerando assim conformações múltiplas que estabilizam a molécula.
Ou seja, o elo central da molécula gira como um cilindro rotativo, alternando consecutivamente o arranjo espacial dos grupos – COOH, H e OH (projeções de Newman).
Por exemplo, na imagem os dois grupos OH apontam em direções opostas, o que significa que eles estão em posições um contra o outro. O mesmo vale para os grupos –COOH.
Outra possível conformação é a de um par de grupos eclipsados, nos quais os dois grupos são orientados na mesma direção. Essas conformações não teriam um papel importante na estrutura do composto se todos os grupos de carbonos C 2 e C 3 fossem iguais.
Como neste composto, os quatro grupos são diferentes (–COOH, OH, H e o outro lado da molécula), os carbonos são assimétricos (ou quirais) e exibem a famosa atividade óptica.
A maneira pela qual os grupos nos carbonos C 2 e C 3 do ácido tartárico são organizados determina algumas estruturas e propriedades diferentes para o mesmo composto; isto é, permite a existência de estereoisômeros.
Aplicações
Na indústria alimentícia
É usado como estabilizador de emulsão em padarias. Também é usado como ingrediente de levedura, geléia, gelatina e refrigerantes. Também serve como agente acidificante, fermentador e sequestrante de íons.
O ácido tartárico é encontrado nesses alimentos: biscoitos doces, balas, chocolates, líquidos gasosos, produtos de panificação e vinhos.
Na vinificação, é usado para torná-los mais equilibrados, do ponto de vista do sabor, diminuindo o pH.
Na indústria farmacêutica
É utilizado na criação de comprimidos efervescentes, antibióticos e comprimidos, bem como em medicamentos utilizados no tratamento de doenças cardíacas.
Na indústria química
É usado na fotografia, bem como na galvanotecnia e é um antioxidante ideal para gorduras industriais.
Também é usado como um sequestrante de íons metálicos. Como Girando suas ligações de forma a localizar os átomos de oxigênio do grupo carbonila, ricos em elétrons, em torno dessas espécies carregadas positivamente.
Na indústria da construção
Atrasa o processo de endurecimento do gesso, cimento e gesso, tornando mais eficiente o manuseio desses materiais.
Propriedades
– O ácido tartárico é comercializado como um pó cristalino ou cristais brancos levemente opacos. Tem um sabor agradável, e esta propriedade é indicativa de um vinho de boa qualidade.
– Derrete a 206 ºC e queima a 210 ºC. É muito solúvel em água, álcoois, soluções básicas e bórax.
– Sua densidade é de 1,79 g / mL a 18 ° C e possui duas constantes de acidez: pKa 1 e pKa 2 . Ou seja, cada um dos dois prótons ácidos tem sua própria tendência a ser liberada no meio aquoso.
– Como possui grupos –COOH e OH, pode ser analisado por espectroscopia no infravermelho (IR) para suas determinações qualitativas e quantitativas.
– Outras técnicas, como espectroscopia de massa e ressonância magnética nuclear, permitem análises anteriores sobre este composto.
Estereoquímica
O ácido tartárico foi o primeiro composto orgânico ao qual se desenvolveu uma resolução enantiomérica. O que isso significa? Isso significa que seus estereoisômeros poderiam ser separados manualmente, graças ao trabalho de pesquisa do bioquímico Louis Pasteur, em 1848.
E quais são os estereoisômeros do ácido tartárico? São eles: (R, R), (S, S) e (R, S). R e S são as configurações espaciais dos carbonos C 2 e C 3 .
O ácido tartárico (R, R), o mais “natural”, gira a luz polarizada para a direita; O ácido tartárico (S, S) gira no sentido anti-horário, anti-horário. E, finalmente, o ácido tartárico (R, S) não gira a luz polarizada, sendo opticamente inativo.
Louis Pasteur, com a ajuda de um microscópio e uma pinça, encontrou e separou cristais de ácido tartárico que mostravam padrões “destros” e “canhotos”, como na imagem acima.
Assim, os cristais “destros” são aqueles formados pelo enantiômero (R, R), enquanto os cristais “esquerdos” são os do enantiômero (S, S).
No entanto, os cristais de ácido tartárico (R, S) não diferem dos demais, pois exibem características de canhoto e canhoto ao mesmo tempo; portanto, eles não puderam ser “resolvidos”.
Referências
- Monica Yichoy (7 de novembro de 2010). Sedimentos em vinho. [Figura]. Recuperado de: flickr.com
- Wikipedia (2018). Ácido tartárico Recuperado em 6 de abril de 2018, de: en.wikipedia.org
- PubChem (2018). Ácido tartárico. Recuperado em 6 de abril de 2018, de: pubchem.ncbi.nlm.nih.gov.
- Compreendendo tartaratos de vinho. Recuperado em 06 de abril de 2018, de: jordanwinery.com
- Acipedia Ácido tartárico. Recuperado em 6 de abril de 2018, de: acipedia.org
- Pochteca Ácido tartárico Recuperado em 06 de abril de 2018, de: pochteca.com.mx
- Dhaneshwar Singh et al. (2012). Sobre a origem da inatividade óptica do ácido mesotartárico. Departamento de Química, Universidade de Manipur, Canchipur, Imphal, Índia. J. Chem. Pharm. Res., 4 (2): 1123-1129.