Os aldeídos são compostos orgânicos que possuem o grupo funcional -CHO em sua estrutura molecular. Eles são caracterizados pela presença de um carbono ligado a um átomo de hidrogênio e a um grupo carbonila. Os aldeídos apresentam propriedades físicas e químicas únicas, como odor característico, solubilidade em água e reatividade em reações de oxidação e redução.
Os aldeídos são amplamente utilizados na indústria química como intermediários na síntese de diversos compostos orgânicos, como álcoois, ácidos carboxílicos e ésteres. Além disso, eles são empregados na produção de resinas, plásticos, perfumes e aromatizantes. Alguns exemplos de aldeídos conhecidos são o formaldeído, o acetaldeído e o benzaldeído. Em resumo, os aldeídos desempenham um papel fundamental em diversas aplicações industriais e químicas devido às suas propriedades e reatividade únicas.
Como é formada a estrutura do aldeído?
Os aldeídos são compostos orgânicos que possuem um grupo funcional formado por um átomo de carbono ligado a um átomo de hidrogênio e a um grupo carbonila, onde o oxigênio está ligado a um átomo de carbono. A estrutura do aldeído pode ser representada pela fórmula geral RCHO, onde R representa um grupo orgânico.
No caso dos aldeídos comuns, como o formaldeído, o grupo funcional é -CHO. A ligação dupla entre o oxigênio e o carbono confere ao grupo carbonila características únicas, como a capacidade de reagir facilmente com nucleófilos. Além disso, os aldeídos apresentam um ponto de ebulição mais baixo em comparação com os álcoois e cetonas, devido à ausência de ligações de hidrogênio intermoleculares.
Em relação à sua estrutura química, os aldeídos são compostos lineares que podem ser ramificados ou não. Os átomos de oxigênio e hidrogênio estão ligados ao carbono da carbonila, conferindo uma geometria planar ao grupo funcional. Essa estrutura planar permite que os aldeídos participem de reações de adição e oxidação, sendo amplamente utilizados na indústria química e na síntese de diversos compostos.
Características das substâncias aldeídicas: quais são as propriedades específicas desses compostos orgânicos?
Os aldeídos são compostos orgânicos que possuem em sua estrutura o grupo funcional -CHO, conhecido como grupo carbonila. Esses compostos apresentam algumas características específicas que os distinguem de outros compostos orgânicos.
Uma das principais propriedades dos aldeídos é o cheiro característico, muitas vezes descrito como um odor adocicado e penetrante. Além disso, eles são facilmente oxidáveis, podendo se transformar em ácidos carboxílicos por meio de reações de oxidação.
Os aldeídos também possuem pontos de ebulição mais baixos em comparação com os álcoois e cetonas de massa molecular semelhante. Isso ocorre devido à ausência de ligações de hidrogênio intermoleculares nos aldeídos, o que resulta em uma menor força de atração entre as moléculas.
Alguns aldeídos são utilizados na indústria de fragrâncias e aromas, devido ao seu cheiro agradável e característico. Além disso, eles também são empregados na produção de plásticos, resinas e produtos químicos.
Alguns exemplos de aldeídos incluem o formaldeído, acetaldeído e benzaldeído. Cada um desses compostos possui propriedades e aplicações específicas na indústria e na química orgânica.
Identificação de aldeídos: métodos e técnicas para reconhecimento desses compostos orgânicos.
Os aldeídos são compostos orgânicos que possuem o grupo funcional -CHO em sua estrutura química. Para identificar a presença de aldeídos em uma amostra, existem diversos métodos e técnicas disponíveis.
Um dos métodos mais comuns para identificação de aldeídos é a reação de Tollens. Neste teste, o aldeído reage com o reagente de Tollens (nitrato de prata em solução aquosa de amônia) para formar um espelho de prata no tubo de ensaio, indicando a presença do grupo funcional aldeído.
Outra técnica utilizada para reconhecimento de aldeídos é a reação de Fehling. Neste teste, o aldeído reage com o reagente de Fehling (solução de sulfato de cobre e tartrato de potássio) para formar um precipitado de óxido de cobre (I), indicando a presença do grupo aldeído na amostra.
Além desses métodos específicos, a espectroscopia de ressonância magnética nuclear (RMN) e espectroscopia no infravermelho (IV) também podem ser utilizadas para identificar a presença de aldeídos em uma amostra, através da análise dos deslocamentos químicos e bandas características desses compostos.
Em resumo, a identificação de aldeídos pode ser feita através de métodos como a reação de Tollens, reação de Fehling, espectroscopia de RMN e espectroscopia no IV. Essas técnicas são essenciais para reconhecer e caracterizar compostos orgânicos que contenham o grupo funcional aldeído em sua estrutura.
Nomenclatura dos aldeídos: como nomear esses compostos orgânicos de forma correta.
Os aldeídos são compostos orgânicos que possuem o grupo funcional -CHO, também conhecido como grupo carbonila. Para nomear corretamente esses compostos, é importante seguir algumas regras de nomenclatura.
Para nomear um aldeído, primeiro identificamos a cadeia principal, que contém o grupo carbonila. Em seguida, substituímos a terminação “-o” do hidrocarboneto correspondente pela terminação “-al”. Por exemplo, o aldeído formado por uma cadeia de três átomos de carbono é chamado de propanal.
Quando a cadeia principal possui ramificações, utilizamos os prefixos metil-, etil-, propil-, entre outros, para indicar a posição dessas ramificações em relação ao grupo carbonila. Por exemplo, o nome do aldeído a seguir é 2-metilbutanal.
É importante destacar que, em alguns casos, é necessário indicar a posição do grupo carbonila na cadeia principal. Para isso, utilizamos os números dos átomos de carbono onde o grupo está ligado. Por exemplo, o aldeído com um grupo carbonila ligado ao segundo átomo de carbono é chamado de butanal.
Portanto, a nomenclatura dos aldeídos segue essas regras básicas para garantir a correta identificação e nomeação desses compostos orgânicos.
Aldeídos: estrutura, propriedades, usos e exemplos
Os aldeídos são os compostos orgânicos que possuem a fórmula geral RCHO. R representa uma cadeia alifática ou aromática; C para carbono; Ou ao oxigênio e H ao hidrogênio. Eles são caracterizados por possuir um grupo carbonil, bem como cetonas e ácidos carboxílicos, de modo que os aldeídos também são chamados de compostos carbonil.
O grupo carbonil fornece ao aldeído muitas de suas propriedades. São compostos que oxidam facilmente e são muito reativos às adições nucleofílicas. A ligação dupla do grupo carbonila (C = O) possui dois átomos que apresentam diferenças em sua avidez por elétrons ( eletronegatividade ).
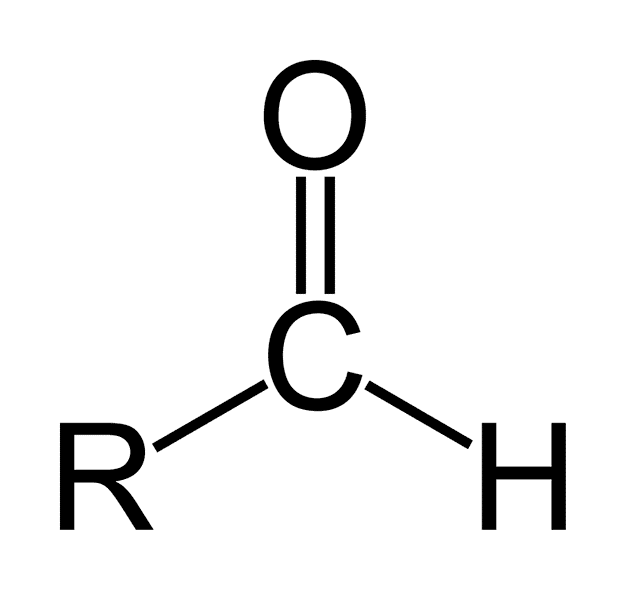
O oxigênio atrai os elétrons mais fortemente que o carbono, de modo que a nuvem eletrônica se move em sua direção, tornando a dupla ligação entre o carbono e o oxigênio na natureza polar, com um importante momento dipolar. Isso produz compostos polares de aldeídos.
A polaridade dos aldeídos influenciará suas propriedades físicas. O ponto de ebulição e a solubilidade dos aldeídos na água são maiores que os compostos químicos não polares com pesos moleculares semelhantes, como é o caso dos hidrocarbonetos.
Aldeídos com menos de cinco átomos de carbono são solúveis em água, uma vez que ligações de hidrogênio se formam entre o oxigênio do grupo carbonil e a molécula de água. No entanto, aumentar o número de carbono da cadeia de hidrocarbonetos produz um aumento na porção não polar do aldeído, tornando-o menos solúvel em água.
Mas como eles são e de onde eles vêm? Embora sua natureza dependa essencialmente do grupo carbonil, o restante da estrutura molecular também contribui muito para o todo. Assim, eles podem ser de qualquer tamanho, pequeno ou grande, ou mesmo uma macromolécula pode ter regiões onde predomina o caráter dos aldeídos.
Assim, como em todos os compostos químicos, existem aldeídos “agradáveis” e outros amargos. Eles podem ser encontrados em fontes naturais ou sintetizados em grandes escalas. Exemplos de aldeídos são a vanilina, muito presente no sorvete (imagem superior) e o acetaldeído, que adiciona sabor às bebidas alcoólicas.
Estrutura quimica
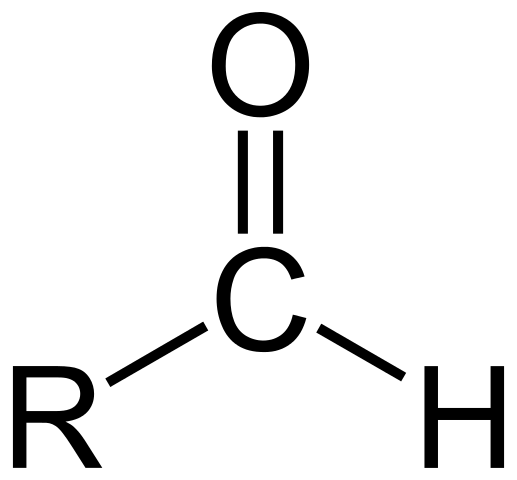
Os aldeídos consistem em um carbonil (C = O) ao qual um átomo de hidrogênio está diretamente ligado. Isto difere de outros compostos orgânicos tais como cetonas (R 2 C = O) e ácidos carboxílicos (RCOOH).
A estrutura molecular em torno do grupo -CHO, formil é mostrada na imagem acima. O grupo formilo é plana, porque o carbono e o oxigénio são hibridao sp 2 . Essa planaridade o torna suscetível ao ataque por espécies nucleofílicas e, portanto, oxida-se facilmente.
A que essa oxidação se refere? À formação de uma ligação com qualquer outro átomo mais eletronegativo que o carbono; e no caso de aldeídos, é um oxigênio. Assim, o aldeído é oxidado a um ácido carboxílico , -COOH. E se o aldeído fosse reduzido? Um álcool primário, ROH, seria formado.
Os aldeídos são produzidos apenas a partir de álcoois primários: aqueles em que o grupo OH está no final de uma cadeia. Da mesma forma, o grupo formil está sempre no final de uma cadeia ou se sobressai dela ou do anel como um substituinte (se houver outros grupos mais importantes, como –COOH).
Propriedades físicas e químicas
Sendo compostos polares, seus pontos de fusão são maiores que os dos compostos não polares. As moléculas de aldeído não são capazes de se ligar intermolecularmente através de ligações de hidrogênio, porque possuem apenas átomos de carbono ligados a átomos de hidrogênio.
Devido ao exposto, os aldeídos têm pontos de ebulição mais baixos que os álcoois e ácidos carboxílicos.
Pontos de fusão
Formaldeído -92; Acetaldeído -121; Propionaldeído -81; n- butiraldeído -99; n-valeraldeído -91; Caproaldeído -; Heptaldeído – 42; Fenilacetaldeído -; Benzaldeído -26.
Pontos de ebulição
Formaldeído -21; Acetaldeído 20; Propionaldeído 49; n-butiraldeído 76; n-valeraldeído 103; Caproaldeído 131; Heptaldeído 155; Fenilacetaldeído 194; Benzaldeído 178.
Solubilidade expressa em g / 100 g de H 2 O
Formaldeído, muito solúvel; Acetaldeído, infinito; Propionaldeído, 16; n-butiraldeído, 7; n-valeraldeído, ligeiramente solúvel; caproaldeído, ligeiramente solúvel; Fenilacetaldeído levemente solúvel; Benzaldeído, 0,3.
Os pontos de ebulição dos aldeídos tendem a aumentar diretamente com o peso molecular. Pelo contrário, existe uma tendência a diminuir a solubilidade dos aldeídos na água à medida que o seu peso molecular aumenta. Isso se reflete nas constantes físicas dos aldeídos mencionados.
Reatividade
Reação de oxidação
Os aldeídos podem ser oxidado para se obter o ácido carboxílico correspondente no a presença de qualquer destes compostos: Ag (NH 3 ) 2 , KMnO 4 ou K 2 Cr 2 O 7 .
Redução para álcoois
Eles podem ser hidrogenados com a ajuda de catalisadores de níquel, platina ou paládio. Assim, C = O é transformado em C-OH.
Redução de hidrocarbonetos
Na presença de Zn (Hg), HCl concentrado ou NH 2 NH 2 aldeídos perder o grupo carbonilo e tornar-se hidrocarbonetos.
Adição Nucleofílica
Existem vários compostos que são adicionados ao grupo carbonil, entre eles estão: reagentes de Grignard, cianeto, derivados de amônia e álcoois.
Nomenclatura
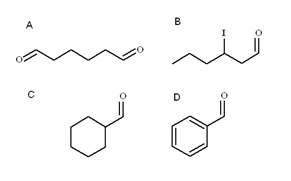
Na imagem acima, quatro aldeídos são ilustrados. Como eles são nomeados?
Como são álcoois primários oxidados, a terminação do álcool é alterada –ol para –al. Assim, metanol (CH 3 OH), se oxidado a CH 3 CHO chamado metanal (formaldeído); CH 3 CH 2 etanal CHO (acetaldeído); CH 3 CH 2 CH 2 propanal CHO e CH 3 CH 2 CH 2 CH 2 butanal CHO.
Todos os aldeídos recém-nomeados possuem o grupo –CHO no final da cadeia. Quando encontrado nas duas extremidades, como em A, a terminação – à qual o prefixo di- é adicionado. Como A possui seis carbonos (contando os de ambos os grupos formil), ele é derivado do 1-hexanol e seu nome é: dial hexano .
Quando há um substituinte, como um radical alquil, uma ligação dupla ou tripla ou um halogênio, os carbonos da cadeia principal são listados dando -CHO o número 1. Assim, o aldeído B é chamado: 3-iodo-hexanal.
No entanto, nos aldeídos C e D, o grupo -CHO não tem prioridade para identificar os referidos compostos de outros. C é um cicloalcano, enquanto D é um benzeno, ambos com um de seus H substituído por um grupo formil.
Neles, como a estrutura principal é cíclica, o grupo formil é denominado carbaldeído. Assim, C é ciclohexanocarbaldeído e D é benzenocarbaldeído (mais conhecido como benzaldeído).
Usos
Existem na natureza aldeídos capazes de conferir sabores agradáveis, como o cinamaldeído, responsável pelo sabor característico da canela. É por isso que eles são frequentemente usados como aromatizantes artificiais em muitos produtos, como doces ou alimentos.
Formaldeído
O formaldeído é o aldeído produzido industrialmente em maior quantidade. O formaldeído obtido pela oxidação do metanol é utilizado em uma solução a 37% do gás na água, sob o nome de formalina. Isso é usado no curtimento de peles e na conservação e embalsamamento de cadáveres.
O formaldeído também é usado como germicida, fungicida e inseticida para plantas e vegetais. No entanto, sua maior utilidade é a contribuição para a produção de material polimérico. O plástico chamado baquelita é sintetizado pela reação entre formaldeído e fenol.
Bakelita
A baquelite é um polímero de estrutura tridimensional de grande dureza usado em vários utensílios domésticos, como cabo de panelas, frigideiras, cafeteiras, facas, etc.
Os polímeros do tipo baquelite são feitos de formaldeído em combinação com os compostos de uréia e melamina. Esses polímeros são usados não apenas como plásticos, mas também como colas adesivas e material de revestimento.
Contraplacado
Contraplacado é o nome comercial de um material formado por finas folhas de madeira, unidas por polímeros produzidos a partir de formaldeído. As marcas Formica e Melmac são fabricadas com a sua participação. A fórmica é um material plástico usado no revestimento de móveis.
O plástico Melmac é usado na preparação de pratos, copos, xícaras, etc. O formaldeído é uma matéria-prima para a síntese do composto diisocianato de metileno difenil (MDI), um precursor do poliuretano.
Poliuretano
O poliuretano é usado como isolante em geladeiras e freezers, estofamento de móveis, colchões, revestimentos, adesivos, solas, etc.
Butiraldeído
O butiraldeído é o principal precursor da síntese de 2-etilhexanol, usado como plastificante. Possui um agradável aroma de maçã que permite seu uso em alimentos como aromatizante.
Também é usado para a produção de aceleradores de borracha. Intervém como reagente intermediário na fabricação de solventes.
Acetaldeído
O acetaldeído foi utilizado na produção de ácido acético. Mas essa função do acetaldeído diminuiu em importância, uma vez que foi deslocada pelo processo de carbonilação do metanol.
Síntese
Outros aldeídos são precursores de oxoálcoois, que são utilizados na produção de detergentes. Os chamados oxoálcoois são preparados adicionando monóxido de carbono e hidrogênio a uma olefina para obter um aldeído. E finalmente o aldeído é hidrogenado para obter o álcool.
Alguns aldeídos são utilizados na fabricação de perfumes, como é o caso da Chanel nº 5. Muitos aldeídos naturais têm odores agradáveis, por exemplo: o heptanal tem um cheiro de grama verde; o octanal um cheiro de laranja; o nonanal, um cheiro de rosas, e o citral, um cheiro de limão.
Exemplos de aldeído
Glutaraldeído

O glutaraldeído possui dois grupos formil em sua estrutura nas duas extremidades.
Comercializado sob o nome de Cidex ou Glutaral, é usado como desinfetante para esterilizar instrumentos cirúrgicos. É utilizado no tratamento de verrugas nos pés, aplicado como líquido. Também é usado como agente de fixação de tecidos em laboratórios de histologia e patologia.
Benzaldeído
É o aldeído aromático mais simples que é formado por um anel benzeno no qual um grupo formil está ligado.
É encontrado no óleo de amêndoa, daí o seu cheiro característico que permite que seja usado como aromatizante de alimentos. Além disso, é utilizado na síntese de compostos orgânicos relacionados à fabricação de medicamentos e na fabricação de plásticos.
Gliceraldeído
É uma aldotriose, um açúcar composto por três átomos de carbono. Possui dois isômeros chamados enantiômeros D e L. O gliceraldeído é o primeiro monossacarídeo obtido na fotossíntese durante a fase escura (ciclo de Calvin).
Gliceraldeído-3-fosfato
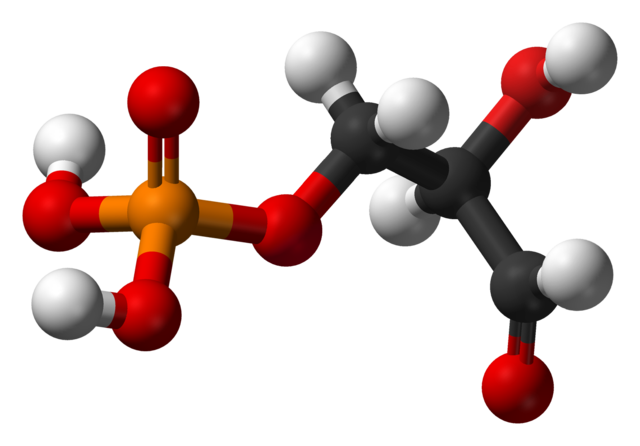
A estrutura do gliceraldeído-3-fosfato é ilustrada na imagem acima. As esferas vermelhas próximas ao amarelo correspondem ao grupo fosfato, enquanto as pretas o esqueleto de carbono. A esfera vermelha ligada ao branco é o grupo OH, mas quando está ligada à esfera preta e a última ao branco, então é o grupo CHO.
O gliceraldeído-3-fosfato está envolvido na glicólise , um processo metabólico no qual a glicose é degradada em ácido pirúvico com a produção de ATP, um reservatório energético de seres vivos . Além disso, a partir da produção de NADH, um agente redutor biológico.
Na glicólise, o gliceraldeído-3-fosfato e o di-hidroacetona fosfato são originários da clivagem de D-frutose-1-6-bifosfato
O gliceraldeído-3-fosfato está envolvido no processo metabólico conhecido como ciclo das pentoses. Isso gera o NADPH, um importante redutor biológico.
11-cis-retinal

O Β-caroteno é um pigmento natural presente em vários vegetais, especialmente cenouras. Ele experimenta uma quebra oxidativa no fígado, transformando-se em álcool retinol ou vitamina A. A oxidação da vitamina A e a subsequente isomerização de uma de suas ligações duplas formam o aldeído 11-cis-retiniano.
Fosfato de piridoxal (vitamina B6)
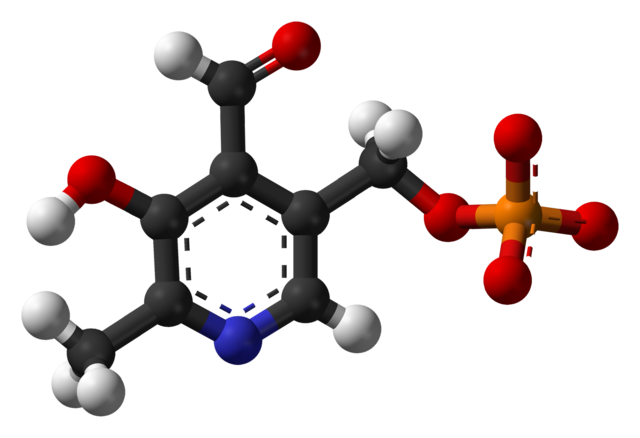
É um grupo protético ligado a várias enzimas, que é a forma ativa da vitamina B6 e participa do processo de síntese do neurotransmissor inibitório do GABA .
Onde está o grupo formil em sua estrutura? Observe que isso difere do restante dos grupos vinculados ao anel aromático.
Salicilaldeído
É uma matéria-prima para a síntese do ácido acetilsalicílico, um medicamento analgésico e antipirético conhecido como aspirina.
Referências
- Robert C. Neuman, Jr. Capítulo 13, Compostos carbonílicos: cetonas, aldeídos, ácidos carboxílicos. [PDF]. Retirado de: chem.ucr.edu
- Germán Fernández. (14 de setembro de 2009). Nomenclatura dos aldeídos. Retirado de: quimicaorganica.net
- TW Graham Solomons, Craigh B. Fryhle. Química Orgânica (Décima Edição, p. 729-731) Wiley Plus.
- Jerry March e William H. Brown. (31 de dezembro de 2015). Aldeído Retirado de: britannica.com
- Wikipedia (2018). Aldeídos Retirado de: https://en.wikipedia.org/wiki/Aldehyde
- Morrison, RT e Boyd, RN (1990). Quinta Edição de Química Orgânica. Editorial Addison-Wesley Iberoamericana.
- Carey, FA (2006). Sexta edição da Organic Chemistry. Editorial Mc Graw Hill.
- Mathews, Ch. K., Van Holde, KE e Athern, KG (2002). Bioquímica Terceira Edição Pearson Adisson Wesley.