CHON é uma sigla que representa os quatro elementos químicos mais abundantes nos seres vivos: carbono (C), hidrogênio (H), oxigênio (O) e nitrogênio (N). Esses elementos são essenciais para a formação das moléculas biológicas e desempenham papéis fundamentais na estrutura e função dos organismos vivos. Suas características comuns incluem a capacidade de formar ligações covalentes, o que permite a criação de moléculas complexas como proteínas, carboidratos, lipídios e ácidos nucleicos. Além disso, cada um desses elementos possui particularidades únicas que influenciam suas interações dentro dos sistemas biológicos. Juntos, CHON desempenham um papel crucial na química da vida e na sustentação da diversidade e complexidade dos organismos vivos.
Conheça os diferentes tipos de moléculas existentes na natureza e suas características.
O CHON é um grupo de moléculas que contêm os elementos carbono, hidrogênio, oxigênio e nitrogênio. Esses elementos são essenciais para a vida na Terra e estão presentes em diversas substâncias orgânicas. As moléculas que pertencem ao grupo CHON compartilham algumas características comuns, como a capacidade de formar ligações covalentes estáveis e a participação em reações bioquímicas fundamentais.
Uma das particularidades das moléculas CHON é a sua diversidade estrutural. Elas podem apresentar diferentes arranjos de átomos, o que resulta em propriedades físicas e químicas distintas. Por exemplo, a molécula de DNA é composta por uma sequência específica de nucleotídeos que contêm os elementos CHON, sendo responsável pela transmissão de informações genéticas.
Outro exemplo de molécula CHON é a hemoglobina, uma proteína presente nos glóbulos vermelhos que transporta oxigênio dos pulmões para os tecidos do corpo. A hemoglobina contém átomos de ferro ligados a um grupo heme, que por sua vez contém os elementos CHON.
Em resumo, as moléculas CHON são fundamentais para a vida na Terra, pois estão envolvidas em processos vitais como a replicação do DNA, o transporte de oxigênio e a produção de energia. Ao conhecer os diferentes tipos de moléculas existentes na natureza e suas características, podemos compreender melhor a complexidade e a diversidade dos sistemas biológicos.
O que são moléculas e qual sua definição no estudo da química?
Moléculas são formadas por átomos ligados entre si por ligações químicas. Elas são a menor unidade de uma substância que apresenta suas propriedades químicas. No estudo da química, as moléculas desempenham um papel fundamental, pois são responsáveis por determinar as características e comportamentos das substâncias.
Quando falamos das moléculas que contêm os elementos CHON (carbono, hidrogênio, oxigênio e nitrogênio), podemos observar algumas características comuns e particularidades. Por exemplo, esses elementos são essenciais para a formação de moléculas orgânicas, que são a base da vida na Terra.
Algumas moléculas que contêm os elementos CHON são fundamentais para os seres vivos, como o DNA e as proteínas. O DNA é responsável por armazenar as informações genéticas dos organismos, enquanto as proteínas desempenham diversas funções vitais, como a catalisação de reações químicas e a estruturação das células.
Portanto, as moléculas que contêm os elementos CHON são essenciais para a vida e desempenham papéis cruciais nos processos biológicos. Estudar essas moléculas e compreender suas propriedades é fundamental para avançar no conhecimento da química e da vida em si.
Qual a ligação entre átomos e moléculas: entenda a química por trás dessa relação.
Os átomos são as unidades básicas da matéria, formadas por um núcleo composto de prótons e nêutrons, ao redor do qual giram elétrons. Quando dois ou mais átomos se combinam, formam as moléculas. Essa ligação entre átomos ocorre por meio de ligações químicas, como a ligação iônica, covalente ou metálica.
No caso dos elementos químicos mais comuns na natureza, como o CHON (carbono, hidrogênio, oxigênio e nitrogênio), é possível observar características comuns e particularidades em suas moléculas. O carbono, por exemplo, é conhecido por sua capacidade de formar longas cadeias carbônicas, que são a base de compostos orgânicos como os açúcares e os lipídios.
O hidrogênio, por sua vez, é o elemento mais abundante no universo e está presente em grande parte das moléculas orgânicas e inorgânicas. Já o oxigênio é essencial para a vida, participando da respiração celular e formando a água juntamente com o hidrogênio. O nitrogênio, por sua vez, é fundamental para a formação de proteínas e ácidos nucleicos, como o DNA.
Em resumo, a ligação entre átomos e moléculas é fundamental para compreender a química por trás da matéria. Os elementos CHON apresentam características comuns e particularidades que influenciam diretamente a formação de diversas substâncias essenciais para a vida na Terra.
A formação das moléculas: o que elas podem criar e transformar ao nosso redor.
As moléculas são componentes essenciais para a formação e transformação de tudo ao nosso redor. Elas são compostas por átomos que se unem por ligações químicas para criar substâncias diversas. Um grupo de moléculas muito importante para a vida na Terra é o CHON, que representa os elementos carbono, hidrogênio, oxigênio e nitrogênio.
O CHON é encontrado em uma grande variedade de moléculas presentes nos seres vivos, como os carboidratos, lipídios, proteínas e ácidos nucleicos. Essas moléculas desempenham papéis fundamentais em processos biológicos, como a produção de energia, a síntese de estruturas celulares e a transmissão de informações genéticas.
Uma das características comuns do CHON é a sua capacidade de formar ligações fortes e estáveis, o que permite a criação de moléculas complexas e diversificadas. Além disso, esses elementos são essenciais para a química orgânica, uma vez que estão presentes em praticamente todas as moléculas dos seres vivos.
Apesar de suas características comuns, o CHON também apresenta particularidades únicas em cada um dos elementos que o compõem. Por exemplo, o carbono tem a capacidade de formar cadeias longas e ramificadas, enquanto o oxigênio é fundamental para processos de oxidação e redução. Já o nitrogênio é essencial para a formação de ligações peptídicas nas proteínas.
Entre as moléculas mais conhecidas que contêm CHON estão a glicose, o DNA, a hemoglobina e a insulina. Essas substâncias desempenham funções vitais nos organismos vivos e são essenciais para a manutenção da vida.
Em resumo, as moléculas formadas por CHON são fundamentais para a criação e transformação de substâncias em nosso entorno. Seja na natureza, nos alimentos que consumimos ou nos medicamentos que utilizamos, essas moléculas desempenham um papel crucial em processos biológicos e químicos que sustentam a vida no planeta.
CHON: características comuns, particularidades e moléculas
CHON : carbono C, hidrogênio H, oxigênio O e nitrogênio N, são um grupo de elementos químicos que compõem a matéria viva. Devido à sua localização na tabela periódica , esses átomos compartilham características que os tornam adequados para a formação de moléculas orgânicas e covalentes.
Esses quatro elementos químicos formam a maioria das moléculas dos seres vivos , chamados bioelementos ou elementos biogênicos. Eles pertencem ao grupo de bioelementos primários ou principais, porque são encontrados em 95% nas moléculas dos seres vivos.
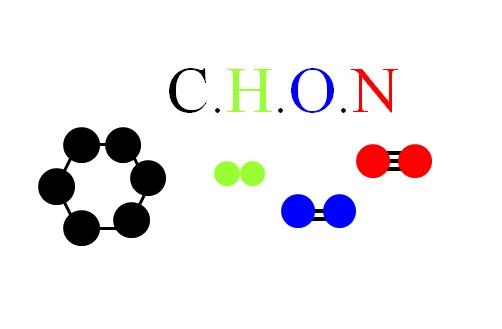
As moléculas e átomos de CHON são mostrados na imagem acima: um anel hexagonal como uma unidade molecular em carbono; a molécula de H 2 (verde); a molécula diatômica do O 2 (azul); e a molécula diatômica de N 2 (vermelho), com sua ligação tripla.
Eles têm parte das propriedades comuns, algumas peculiaridades ou características que explicam por que são adequados para a formação de biomoléculas. Com baixo peso ou massa atômica, isso os torna muito eletronegativos e formam ligações covalentes estáveis, fortes e de alta energia.
Eles se unem como parte da estrutura de biomoléculas orgânicas, como proteínas, carboidratos, lipídios e ácidos nucléicos. Eles também participam da formação de moléculas inorgânicas essenciais para a vida existir; tais como água, H 2 O.
Características comuns de CHON
Massa atômica baixa
Eles têm uma massa atômica baixa. As massas atômicas de C, H, O e N são: 12 u, 1u, 16u e 14u. Isso faz com que eles tenham um raio atômico menor, o que por sua vez lhes permite estabelecer ligações covalentes estáveis e fortes.
Ligações covalentes são formadas quando os átomos que participam da formação das moléculas compartilham seus elétrons de valência.
Ter uma massa atômica baixa e, portanto, um raio atômico menor, torna esses átomos muito eletronegativos.
Alta eletronegatividade
C, H, O e N são muito eletronegativos: atraem fortemente os elétrons que compartilham quando formam ligações dentro de uma molécula.
Todas as propriedades comuns descritas para esses elementos químicos são favoráveis à estabilidade e resistência das ligações covalentes que formam.
As ligações covalentes que se formam podem ser apolares, quando os mesmos elementos são unidos, formando moléculas diatômicas, como o O 2 . Eles também podem ser polares (ou relativamente polares) quando um dos átomos é mais eletronegativo que o outro, como é o caso de O em relação a H.
Esses elementos químicos têm um movimento entre os seres vivos e o ambiente, conhecido como ciclo biogeoquímico na natureza.
Particularidades
Abaixo estão algumas peculiaridades ou propriedades que cada um desses elementos químicos possui que justificam sua função estrutural das biomoléculas.
O átomo de carbono C
-Por sua tetravalência, C pode formar 4 ligações com 4 elementos diferentes ou iguais, formando uma ampla variedade de moléculas orgânicas.
-Pode ser ligado a outros átomos de carbono formando cadeias longas, que podem ser lineares ou ramificadas.
-Também pode formar moléculas cíclicas ou fechadas.
-Você pode formar moléculas com ligações simples, duplas ou triplas. Se na estrutura além de C há H puro, falamos de hidrocarbonetos: alcanos, alcenos e alcinos, respectivamente.
Ao se unir a O, ou N, a ligação adquire polaridade, o que facilita a solubilidade das moléculas que se originam.
– Quando combinado com outros átomos, como O, H e N, forma diferentes famílias de moléculas orgânicas. Pode formar aldeídos, cetonas, álcoois, ácidos carboxílicos, aminas, éteres, ésteres, entre outros compostos.
-As moléculas orgânicas terão diferentes conformações espaciais, as quais estarão relacionadas à funcionalidade ou atividade biológica.
Átomo de H
-Tem o menor número atômico de todos os elementos químicos e combina com o O para formar água.
-Este átomo de H está presente em grande proporção nos esqueletos de carbono que formam as moléculas orgânicas.
– Quanto maior a quantidade de ligações CH nas biomoléculas, maior a energia produzida com sua oxidação. Por esse motivo, a oxidação dos ácidos graxos gera mais energia do que a produzida no catabolismo dos carboidratos.
O átomo de O
É o bioelemento que junto com o H forma a água. O oxigênio é mais eletronegativo que o hidrogênio, o que permite formar dipolos na molécula de água.
Esses dipolos facilitam a formação de fortes interações, chamadas ligações de hidrogênio. Ligações fracas, como pontes H, são essenciais para a solubilidade molecular e para manter a estrutura das biomoléculas.
O átomo de N
-É encontrado no grupo amino de aminoácidos, e no grupo variável de alguns aminoácidos, como histidina, entre outros.
-É essencial para a formação de amino-açúcares, as bases nitrogenadas de nucleotídeos, coenzimas, entre outras moléculas orgânicas.
Moléculas que compõem CHON
A água

H e O são unidos por ligações covalentes formando água na proporção de 2H e um O. Como o oxigênio é mais eletronegativo que o hidrogênio, eles se unem formando uma ligação covalente do tipo polar.
Por ter esse tipo de ligação covalente, permite que muitas substâncias sejam solúveis, formando ligações de hidrogênio com elas. A água faz parte da estrutura de um organismo ou vive em aproximadamente 70 a 80%.
A água é o solvente universal, cumpre muitas funções na natureza e nos seres vivos; Possui função estrutural, metabólica e reguladora. Em meio aquoso, a maioria das reações químicas dos seres vivos é realizada, entre muitas outras funções.
Gases

Por união do tipo apolar covalente, isto é, sem diferença de eletronegatividade, átomos iguais como O. Gases atmosféricos, como nitrogênio e oxigênio molecular, são formados essenciais para o meio ambiente e os seres vivos.
Biomoléculas
![]()
Esses bioelementos se unem e com outros bioelementos, formando as moléculas dos seres vivos.
Eles são unidos por ligações covalentes, dando origem a unidades de monômeros ou moléculas orgânicas simples. Estes, por sua vez, são unidos por ligações covalentes e formam polímeros ou moléculas orgânicas complexas e supramoléculas.
Assim, os aminoácidos formam proteínas e os monossacarídeos são as unidades estruturais dos carboidratos ou carboidratos. Os ácidos graxos e o glicerol formam lipídios saponificáveis e os mononucleotídeos compõem os ácidos nucleicos do DNA e do RNA .
Entre as supramoléculas estão, por exemplo: glicolipídios, fosfolipídios, glicoproteínas, lipoproteínas, entre outros.
Referências
- Carey F. (2006). Quimica Organica. (6a ed.). México, Mc Graw Hill.
- Herói do Curso (2018). 2 função de bioelementos bioelementos primários entre. Recuperado de: coursehero.com
- Chronodon (sf). Bioelementos Recuperado de: cronodon.com
- Pessoa da vida (2018). Bioelementos: Classificação (Primária e Secundária). Recuperado de: lifepersona.com
- Mathews, Holde e Ahern. (2002) Bioquímica (3ª ed.). Madri: PEARSON