O cloreto de alumínio (AlCl3) é um composto químico inorgânico formado por um átomo de alumínio e três átomos de cloro. Possui uma estrutura molecular trigonal planar, onde o átomo de alumínio está no centro e os átomos de cloro estão dispostos ao redor dele.
O cloreto de alumínio é um sólido branco e altamente higroscópico, o que significa que tem a capacidade de absorver umidade do ar. É altamente solúvel em água e reage violentamente com a mesma, sendo corrosivo e irritante para a pele e olhos.
Entre os usos do cloreto de alumínio, destacam-se a sua utilização como coagulante em processos de tratamento de água, na produção de alumínio metálico, na síntese de compostos orgânicos, na fabricação de medicamentos e na indústria de cosméticos. Além disso, é empregado como catalisador em diversas reações químicas, como a alquilação de Friedel-Crafts.
Em resumo, o cloreto de alumínio é um composto químico versátil e amplamente utilizado em diversas aplicações industriais e químicas devido às suas propriedades únicas e reatividade.
Utilizações do cloreto de alumínio na indústria e na medicina: descubra suas aplicações.
O cloreto de alumínio (AlCl3) é um composto químico amplamente utilizado na indústria e na medicina devido às suas diversas aplicações. Com uma estrutura molecular formada por um átomo de alumínio e três átomos de cloro, o AlCl3 possui propriedades únicas que o tornam essencial em muitos processos.
Na indústria, o cloreto de alumínio é frequentemente utilizado como um catalisador em reações químicas, principalmente na produção de plásticos e borrachas. Sua capacidade de acelerar reações e aumentar a eficiência dos processos torna-o um componente-chave em várias cadeias de produção. Além disso, o AlCl3 é empregado na fabricação de produtos farmacêuticos, corantes e explosivos.
Na medicina, o cloreto de alumínio é utilizado como adstringente em formulações tópicas para tratamento de problemas de pele, como acne e dermatite. Sua capacidade de contrair os tecidos e controlar a produção de oleosidade o torna eficaz no combate a várias condições dermatológicas. Além disso, o AlCl3 é empregado em formulações de desodorantes como agente antitranspirante.
Em resumo, o cloreto de alumínio desempenha um papel fundamental tanto na indústria quanto na medicina, sendo essencial para a produção de diversos produtos e para o tratamento de diversas condições de saúde. Suas propriedades únicas e versáteis fazem dele um componente valioso em diferentes setores, garantindo sua relevância e utilização contínuas.
Significado do AlCl3: fórmula química do cloreto de alumínio e suas propriedades.
O cloreto de alumínio, cuja fórmula química é AlCl3, é um composto químico inorgânico muito importante na indústria química. É um sólido branco e altamente higroscópico, o que significa que absorve facilmente a umidade do ar. Isso faz com que o AlCl3 seja utilizado como um agente desidratante em várias reações químicas.
AlCl3 é uma molécula planar, com uma estrutura molecular trigonal planar. Isso significa que o átomo de alumínio está ligado a três átomos de cloro em um mesmo plano. Essa estrutura é responsável por várias propriedades do cloreto de alumínio, como sua alta reatividade e capacidade de atuar como um catalisador em diversas reações químicas.
AlCl3 é amplamente utilizado na indústria química como um catalisador em reações de polimerização, especialmente na produção de plásticos. Além disso, é utilizado na produção de medicamentos, corantes e na síntese de compostos orgânicos. Suas propriedades únicas o tornam uma substância muito versátil e importante na química moderna.
Descubra a natureza da ligação do AlCl3 e suas propriedades químicas.
O Cloreto de Alumínio (AlCl3) é um composto químico de grande importância devido às suas propriedades únicas. Sua estrutura consiste em um átomo de alumínio ligado a três átomos de cloro, formando assim uma ligação covalente. Essa ligação é bastante forte, o que confere ao AlCl3 alta estabilidade.
Em relação às propriedades químicas, o AlCl3 é altamente reativo devido à sua capacidade de aceitar pares de elétrons de outras moléculas. Essa característica faz com que o AlCl3 seja utilizado como um poderoso catalisador em reações orgânicas, principalmente na produção de compostos aromáticos como o tolueno.
Além disso, o AlCl3 é conhecido por sua capacidade de formar complexos com diversas moléculas orgânicas, o que amplia ainda mais suas aplicações na indústria química. Esses complexos são essenciais em processos de polimerização e síntese de compostos químicos de alta complexidade.
Em resumo, o Cloreto de Alumínio (AlCl3) é um composto químico com uma ligação covalente forte, propriedades reativas e um amplo leque de usos na indústria química. Sua capacidade de formar complexos e atuar como catalisador o tornam uma ferramenta essencial para a produção de diversos compostos químicos.
Fórmula química do cloreto de alumínio: qual é e como é formada?
A fórmula química do cloreto de alumínio é AlCl3. Essa substância é formada pela combinação de um átomo de alumínio (Al) e três átomos de cloro (Cl). O alumínio possui uma valência de +3, enquanto o cloro possui uma valência de -1, o que resulta na formação do AlCl3.
Cloreto de Alumínio (AlCl3): estrutura, propriedades, usos
O cloreto de alumínio é um composto inorgânico que possui uma estrutura molecular em que um átomo de alumínio está ligado a três átomos de cloro. Essa estrutura forma um sólido branco e altamente solúvel em água.
Entre as propriedades do cloreto de alumínio, destacam-se sua capacidade de formar complexos com várias moléculas orgânicas, sua alta reatividade e seu papel como catalisador em diversas reações químicas.
Quanto aos usos do cloreto de alumínio, ele é amplamente utilizado na indústria química como catalisador em processos de polimerização, na produção de medicamentos e cosméticos, e também na fabricação de corantes e pigmentos.
Em resumo, o cloreto de alumínio (AlCl3) é um composto químico importante com diversas aplicações na indústria e na pesquisa, devido às suas propriedades únicas e à sua versatilidade como catalisador.
Cloreto de Alumínio (AlCl3): estrutura, propriedades, usos
O cloreto de alumínio , ou tricloreto de alumínio (AlCl 3 ) é um sal de binário formado por alumínio e cloro. Às vezes, é apresentado como um pó amarelo porque possui impurezas devido à presença de cloreto de ferro (III).
É obtido pela combinação de seus elementos. O alumínio, que possui três elétrons em seu último nível de energia (família IIIA), devido ao seu caráter metálico tende a produzi-los. O cloro com sete elétrons em seu último nível de energia (família VIIA) tende a ganhá-los para completar seu octeto.
Considera-se que a ligação formada entre o alumínio e o cloro no tricloreto de alumínio é covalente, embora seja a união entre um metal e um não-metal.
Existem dois tipos de cloreto de alumínio:
- Cloreto de alumínio anidro. AlCl 3.
- Hexa-hidrato de cloreto de alumínio. AlCl 3 . 6H 2 O. Este composto pode ser encontrado na forma sólida ou em solução.
Estrutura quimica
tricloreto de alumínio anidro, é uma molécula com uma geometria planar triangular com um ângulo de 120 ° correspondendo a uma sp hibridado atómica 2 .
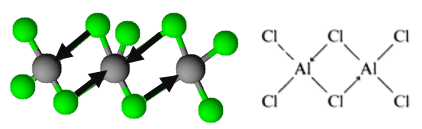
No entanto, a molécula é organizada na forma de dímeros , nos quais um átomo de cloro doa um par de elétrons para formar ligações. Estes são conhecidos como ligações covalentes coordenadas.
É assim que se deduz a organização dos dímeros do tricloreto de alumínio.
Essa organização permite que o composto se forme em redes de camadas diméricas. Quando a água é vertida sobre tricloreto de alumínio sólido, eles não se dissociam como esperado dos compostos iônicos, mas sofrem hidrólise vigorosa.
Em contraste, em solução aquosa diluída de iões são coordenados [Al (H 2 O) 6 ] 3 e cloreto. Essas estruturas são muito semelhantes às do diborano.
Desta forma, temos a fórmula Al 2 Cl 6
Se a diferença na eletronegatividade dos átomos que formam as ligações nesse composto for medida, pode-se observar o seguinte:
Para o alumínio Al, o valor da eletronegatividade é 1,61 C e o do cloro é 3,16 C. A diferença na eletronegatividade é 1,55 C.
De acordo com as regras da teoria das ligações, para que um composto seja iônico, ele deve ter uma diferença na eletronegatividade dos átomos que compõem a ligação de um valor maior ou igual a 1,7 C.
No caso da ligação Al-Cl, a diferença na eletronegatividade é de 1,55 C, o que confere ao tricloreto de alumínio um arranjo de ligação covalente. Este pequeno valor pode ser atribuído às ligações covalentes coordenadas que a molécula apresenta.
Propriedades
Física
Aparência : sólido branco, às vezes de cor amarela devido a impurezas causadas pelo cloreto férrico
Densidade : 2,48 g / mL
Massa molar : 133.34 g / mol
Sublimação : sublime a 178 ° C, portanto seus pontos de fusão e ebulição são muito baixos.
Dirigir : conduz mal a eletricidade.
Solubilidade : não é solúvel em água porque é um ácido de Lewis.É solúvel em solventes orgânicos como benzeno, tetracloreto de carbono e clorofórmio.
Química
Na água, o tricloreto de alumínio é hidrolisado para formar HCl e íon hidrônio e hidróxido de alumínio:
É usado nas reações de Friedel-Crafts como um catalisador (uma substância que pode ser recuperada no final da reação, porque está apenas nela para acelerar, retardar ou iniciar uma reação).
É uma substância corrosiva.
Na decomposição, quando reage violentamente com a água, produz óxido de alumínio e gases perigosos, como o cloreto de hidrogênio.
Usos
- Antitranspirante
- Catalisador de acilação e alquilação de Friedel-Crafts.
Riscos: possíveis efeitos
- É uma substância corrosiva, causa queimaduras na pele e danos oculares graves.
- Reage violentamente com a água.
- É perigoso para o meio ambiente.
- Muito tóxico para os organismos aquáticos.
Recomendações
Evite a exposição ao produto sem as medidas de segurança necessárias. Deve ser usado, óculos de segurança, luvas, roupas adequadas, sapato coberto.
Em caso de inalação . A inalação de poeira pode irritar o trato respiratório devido à natureza corrosiva da substância. Os sintomas incluem dor de garganta, tosse e falta de ar. Os sintomas do edema pulmonar podem ser tardios e os casos graves podem ser fatais. Mova a vítima para um local arejado sem contaminantes. forneça respiração artificial, se necessário. Se você tiver dificuldade respiratória, forneça oxigênio. Ligue para o médico.
Em caso de contato com a pele . O AlCl 3 é corrosivo. Pode causar irritação ou queimaduras com vermelhidão e dor. Lave imediatamente após contato com água em abundância, por pelo menos 20 minutos. Não neutralize ou adicione outras substâncias além da água. Remova a roupa contaminada e lave-a antes de reutilizá-la. Verifique imediatamente com o seu médico se foram causados ferimentos.
Em contato com os olhos . O AlCl 3 é corrosivo. Causa dor intensa, visão turva e danos nos tecidos. Lave imediatamente os olhos com água por pelo menos 20 minutos e mantenha as pálpebras abertas para garantir que todo o olho e os tecidos das pálpebras estejam limpos. Lavar os olhos em questão de segundos é essencial para obter a máxima eficácia. Se você tiver lentes de contato, tire-as após os primeiros 5 minutos e continue enxaguando os olhos. Consulte o médico. Pode causar sérios danos à córnea, conjuntiva ou outras partes do olho.
Em caso de ingestão . O AlCl 3 é corrosivo. A combustão pode causar dor na boca e esôfago e queimaduras das mucosas. Pode causar desconforto gastrointestinal com dor abdominal, náusea, vômito e diarréia. NÃO provoque vômito. Lave a boca e beba água. Nunca dê nada por via oral a uma pessoa inconsciente. Ligue para o médico. Se o vômito ocorrer espontaneamente, coloque a vítima de lado para reduzir o risco de aspiração.
Pessoas com distúrbios cutâneos existentes ou problemas oculares ou função respiratória comprometida podem ser mais suscetíveis aos efeitos da substância
A embalagem e o armazenamento do composto AlCl 3 devem ser feitos em locais ventilados, limpos e secos.
Referências
- Livro químico, (2017), Cloreto de alumínio. Recuperado de chemicalbook.com
- cosmos online, cosmos.com.mx
- Sharpe, AG, (1993), Química Orgánica, Espanha, Editorial Reverté, SA
- F., (2017), AlCl 3 Cloreto de Alumínio , El Insignia. Retirado de blog.elinsignia.com.
- TriHealth, (2018), Tricloreto de alumínio, última atualização, 4 de março de 2018, Recuperado de trihealth.adam.com.
- RxWiki, (sf), cloreto de alumínio, recuperado de, rxwiki.com.