Heptoses são carboidratos de sete carbonos encontrados em algumas bactérias, fungos e plantas. São considerados açúcares raros devido à sua menor ocorrência em comparação com os hexoses e pentoses. Apesar de sua baixa abundância, as heptoses desempenham um papel crucial em várias vias metabólicas e processos biológicos, como a biossíntese de lipopolissacarídeos em bactérias e a regulação da expressão gênica em plantas. A síntese de heptoses é um processo complexo que envolve várias etapas enzimáticas e requer a ativação de precursores específicos. O estudo das heptoses é importante não apenas para compreender melhor a bioquímica e biologia celular, mas também para o desenvolvimento de novas terapias e tratamentos médicos.
Principais características dos carboidratos: o que você precisa saber sobre esses nutrientes essenciais.
Os carboidratos são macronutrientes essenciais para o nosso organismo, sendo uma importante fonte de energia para as células. Eles são compostos por carbono, hidrogênio e oxigênio, e podem ser classificados em monossacarídeos, dissacarídeos e polissacarídeos.
Os monossacarídeos são os carboidratos mais simples, como a glicose e a frutose. Já os dissacarídeos são formados pela união de dois monossacarídeos, como a sacarose e a lactose. Os polissacarídeos são compostos por muitas unidades de monossacarídeos, como o amido e a celulose.
Os carboidratos desempenham diversas funções no organismo, além de fornecer energia, como reserva energética, estrutura de células e tecidos, participação na comunicação celular, entre outras. É importante manter um equilíbrio na ingestão de carboidratos, optando por fontes saudáveis como frutas, legumes, cereais integrais e leguminosas.
Heptoses: características, importância biológica, síntese.
As heptoses são carboidratos compostos por sete átomos de carbono em sua estrutura. Elas desempenham um papel fundamental em diversos processos biológicos, atuando na síntese de compostos importantes para o organismo.
Uma das principais funções das heptoses é participar da formação de lipopolissacarídeos, que são componentes da parede celular de bactérias gram-negativas. Esses compostos são essenciais para a integridade da parede celular e para a interação com o ambiente externo.
A síntese de heptoses ocorre por meio de vias metabólicas específicas que envolvem diversas enzimas e etapas. É um processo complexo, mas essencial para a produção desses carboidratos no organismo.
Sua síntese é um processo complexo, mas fundamental para o funcionamento adequado do organismo.
Características principais dos polissacarídeos: o que você precisa saber sobre eles.
Os polissacarídeos são macromoléculas formadas por longas cadeias de monossacarídeos ligados entre si por ligações glicosídicas. Eles desempenham diversas funções nos seres vivos, como reserva de energia, estrutura celular e comunicação celular. Alguns exemplos de polissacarídeos são o amido, a celulose e o glicogênio.
Heptoses são um tipo de monossacarídeo que possuem sete átomos de carbono em sua estrutura. Eles são menos comuns do que os hexoses e pentoses, mas desempenham um papel importante em processos biológicos específicos. Um exemplo de heptose é a sedoheptulose, que está presente na via das pentoses fosfato.
As heptoses são essenciais para a síntese de diversas moléculas importantes para os seres vivos, como nucleotídeos, vitaminas e outros compostos bioativos. Sua presença em vias metabólicas específicas mostra a importância desses monossacarídeos para o funcionamento adequado das células.
Apesar de menos comuns, as heptoses desempenham um papel importante em processos biológicos específicos, como a síntese de nucleotídeos e vitaminas.
Principais funções biológicas dos carboidratos e exemplos de sua atuação no organismo humano.
Os carboidratos são moléculas essenciais para o funcionamento do organismo humano, desempenhando diversas funções biológicas. Uma das principais funções dos carboidratos é fornecer energia para as células, sendo a principal fonte de combustível para o corpo. Além disso, eles também desempenham um papel estrutural, formando parte da composição de células e tecidos.
Um exemplo da atuação dos carboidratos no organismo humano é a glicose, um monossacarídeo que é a principal fonte de energia para as células. A glicose é obtida a partir da metabolização de carboidratos presentes nos alimentos e é utilizada pelas células para realizar suas funções metabólicas.
Além disso, os carboidratos também desempenham um papel importante no sistema imunológico, atuando como reconhecedores de agentes patogênicos e facilitando a resposta do organismo a infecções.
Heptoses: características, importância biológica, síntese
As heptoses são um tipo de carboidrato composto por sete átomos de carbono em sua estrutura. Elas são menos comuns do que os carboidratos de seis carbonos, como a glicose, mas desempenham um papel importante em diversos processos biológicos.
Uma das principais características das heptoses é a sua participação na síntese de lipopolissacarídeos, que são componentes da parede celular de algumas bactérias. Esses lipopolissacarídeos são importantes para a proteção das bactérias contra agentes externos e também desempenham um papel na interação desses microorganismos com o sistema imunológico do hospedeiro.
Além disso, as heptoses também estão envolvidas na síntese de alguns ácidos nucleicos, como o ácido ribonucleico (RNA), que desempenha um papel fundamental na síntese de proteínas e na regulação genética.
Sua síntese e metabolismo são essenciais para o funcionamento adequado do organismo.
Características e estruturas químicas dos monossacarídeos: o que são e como se apresentam?
Os monossacarídeos são os carboidratos mais simples, compostos por uma única molécula de açúcar. Eles são os blocos de construção dos carboidratos mais complexos, como os dissacarídeos e polissacarídeos. Os monossacarídeos possuem fórmula geral (CH2O)n, onde “n” varia de 3 a 7.
Em termos de estrutura química, os monossacarídeos podem ser classificados de acordo com o número de átomos de carbono que possuem. Os mais comuns são trioses (3 carbonos), tetroses (4 carbonos), pentoses (5 carbonos), hexoses (6 carbonos) e heptoses (7 carbonos).
Heptoses: características, importância biológica, síntese
As heptoses são monossacarídeos compostos por sete átomos de carbono. Embora sejam menos comuns do que os hexoses, as heptoses desempenham um papel crucial em diversas vias metabólicas e processos biológicos. Elas estão presentes em alguns lipopolissacarídeos de bactérias patogênicas, por exemplo.
A síntese de heptoses ocorre através de vias metabólicas específicas, envolvendo diversas enzimas e substratos. Esses compostos são essenciais para o funcionamento adequado de alguns organismos, sendo fundamentais para a manutenção da homeostase.
Suas estruturas químicas e funções biológicas desempenham um papel crucial na fisiologia dos seres vivos.
Heptoses: características, importância biológica, síntese
Os heptoses são monossacarídeos tendo sete átomos de carbono e com a fórmula empírica C 7 H 14 O 7 . Esses açúcares, como outros monossacarídeos, são poli-hidroxilados e podem ser: aldoheptoses, que têm uma função aldeído no carbono um, ou cetoheptoses, que possuem um grupo cetona no carbono 2.
As heptoses são sintetizadas em vias metabólicas, como o ciclo de fotossíntese de Calvin e a fase não oxidativa da via da pentose fosfato. São constituintes dos lipopolissacarídeos (LPS) na parede celular de bactérias Gram-negativas, como Escherichia coli , Klebsiella sp., Neisseria sp., Proteus sp., Pseudomonas sp., Salmonella sp., Shigella sp. E Vibrio sp.
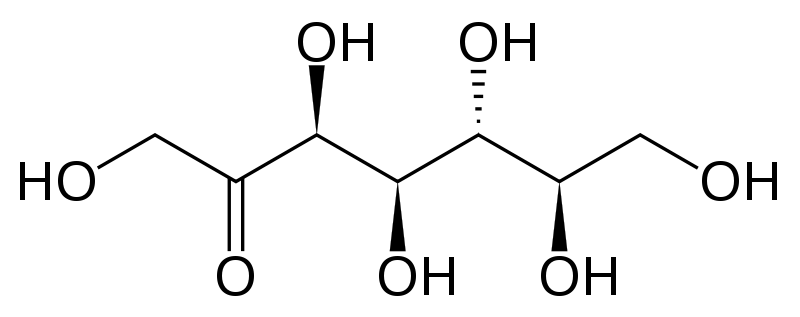
Caracteristicas
Heptoses, semelhantes às hexoses, existem predominantemente em sua forma cíclica. As aldoheptoses possuem cinco carbonos assimétricos e ciclose para formar uma piranose. Por outro lado, as cetoheptoses possuem quatro carbonos assimétricos, onde também formam piranose.
Uma cetoheptose natural muito comum em organismos vivos é a sedoheptulose. Este açúcar é importante na formação de açúcares hexose na fotossíntese e no metabolismo de carboidratos em animais.
Quando a sedoheptulose é aquecida em um ácido mineral diluído, forma uma mistura mineral de equilíbrio, onde 80% é cristalizado como 2,7-anidro- β -D-altro-heptulopiranose e 20% é sedoheptulose.
A determinação química das heptoses é feita com ácido sulfúrico e cisteína, difenilamina e floroglucinol. Sob certas condições, é possível diferenciar heptoses de outros açúcares. Pode até diferenciar entre aldoheptoses e cetoheptoses.
Muitas aldoheptoses têm a configuração gliceric-D-manoheptosa. As heptoses, juntamente com o ácido ceto-açúcar de oito carbonos (ácido 3-desoxi-D-mano-2-octulosônico, um açúcar Kdo), são componentes estruturais do LPS, na membrana externa da bicamada lipídica de bactérias .
O LPS pode ser extraído usando uma mistura de fenol a 45% em água. Em seguida, a KDO heptase e açúcares podem ser identificados por técnicas colorimétricas e cromatográficas.
Importância biológica das heptoses
Na fotossíntese e na via das pentoses fosfato
No estroma do cloroplasto estão as enzimas que convertem os trioses fosfato, gliceraldeído-3-fosfato e di-hidroxiacetona fosfato, produzidos pela assimilação de CO 2 , em amido. A formação de trioses de fosfato e a recuperação de carbonos, para recomeçar a fixação de CO 2 , constituem dois estágios do ciclo de Calvin.
Durante a fase de recuperação de carbono, a enzima aldolase é responsável pela conversão de eritrose 4-fosfato (um metabólito de quatro carbonos (E4P)) e di-hidroxicetona fosfato (um metabólito de três carbonos) em 1,7-bifosfato-sedo-heptulose .
Esta cetoheptose é transformada por vários passos catalisados enzimaticamente em 1,5-bisfosfato de ribulose.
O 1,5-bifosfato de ribulose é o metabólito no início do ciclo de Calvin. Por outro lado, a biossíntese do 7-fosfato de sedo-heptulose (S7P) ocorre na via da pentose fosfato, uma via presente em todos os organismos vivos. Nesse caso, a ação de uma transketolase transforma duas pentoses fosfato em S7P e gliceraldeído-3-fosfato (GAP).
Em seguida, por duas etapas catalisadas por uma transaldolase e uma transketolase, S7P e GAP são transformados em frutose-6-fosfato e GAP. Ambos são metabolitos da glicólise.
Nos lipopolissacarídeos (LPS) de bactérias
As heptoses estão presentes nos lipopolissacarídeos e polissacarídeos da cápsula bacteriana. O motivo estrutural do LPS das enterobactérias consiste no lipídeo A, que consiste em um dímero de 2-amino-2-desoxi-D-glicose ligado pela ligação β- (1®6). Possui dois ésteres de fosfato e grupos de ácidos graxos de cadeia longa.
O lipídeo A está ligado a uma região central por uma ponte de três açúcares Kdo e ácido cetodesoxioctulosônico, ligados por ligações glicosídicas (2®7). Essa região está ligada à L-glicerol-D-manheptosa heptase, com configuração alfa anomérica. Existe uma região O-antigênica.
Esse motivo estrutural está presente em bactérias Gram-negativas, como Escherichia coli , Klebsiella sp., Yersinia sp., Pseudomonas sp., Salmonella sp., Além de outras bactérias patogênicas.
Existem variantes de heptoses que incluem diferentes configurações do estereocentro da piranose em oligossacarídeos, bem como cadeias laterais em polissacarídeos. D-glicerol-D-mão-heptopiranosil está presente em Yersinia enterocolitica , Coxiella burnetti , Mannheimia haemolitica , Aeromonas hydrophila e Vibrio salmonicida .
Heptoses D-glicerina-D-mão-heptoses estão presentes como unidades de cadeia lateral na região externa do LPS de cepas de Proteus e Haemophilus influenzae ; e como cadeias laterais oligoméricas curtas ligadas por α – (1®3) ou α – (1®2), ligadas ao motivo estrutural LPS de Klebsiella pneumonie .
Nas cepas de Vibrio cholerae , a região O-antigênica possui D-glicerol-D-mão-heptose com ambas as configurações anoméricas (alfa e beta).
Em bactérias glicoproteínas
As camadas de sua superfície (camadas S) são compostas por subunidades de proteínas idênticas, que a cobrem em uma organização bidimensional. Eles são encontrados em bactérias e arqueobactérias gram-positivas e gram-negativas. As proteínas nesta camada possuem glicopeptídeos que são alongados por cadeias polissacarídicas.
As glicoproteínas de Aneurinibacillus thermoaerophilus , uma bactéria gram-positiva, têm unidades repetidas de dissacarídeos ®3) -Glicerol- β -D-mão-Hepp- (1®4) – α -L-Rhap- (1® na camada S.
Uma das funções das glicoproteínas é a adesão. Por exemplo, existe uma glicoproteína que mede a adesão como uma proteína autotransportadora (AIDA-I) em cepas de E. coli . A biossíntese de glicoproteínas ocorre através de glicosil transferases, como a heptosil transferase, que necessita de ADP de glicerol-mão-heptosa.
Síntese
A síntese química e a combinação de métodos químicos e enzimáticos das heptoses fosfatadas e hepato-nucleotídicas permitiram elucidar as vias metabólicas usadas pelos microorganismos para produzir essas substâncias.
Muitos métodos sintéticos preparam heptoses manuais 6-epiméricas para sintetizar L-glicerol-D-mão-heptosa. Esses métodos são baseados no alongamento da cadeia do grupo carbono anomérico ou aldeído, usando reagentes de Grignard. As glicosilações são realizadas na presença de grupos protetores de acil.
Assim, há estereoquímico preservando a configuração α -anomérica. Os tioglicosídeos anoméricos e derivados de tricloroacetimidato servem como doadores do grupo heptosil. Os procedimentos mais recentes envolvem a formação seletiva de β- heptósidos e derivados de 6-desoxi-heptósidos.
A biossíntese de heptosas-nucleotídeo ativado inicia-se com 7-fosfato de sedo-heptulose, que é convertido em 7-fosfato de D-glicerina-D-mano-heptosa. Foi proposto numa forma fosfomutase de heptosil fosfato anomérico. Então, uma heptosil transferase catalisa a formação de ADP D-glicero-D-mano-heptosa.
Finalmente, uma epimerase altera a configuração de ADP D-glicerol-D-mão-heptosa para ADP L-glicerina-D-mano-heptosa.
Além disso, estudos químicos foram realizados para conhecer os mecanismos pelos quais essas enzimas realizam a catálise. Por exemplo, eles usam benzilbenzil-manopiranósido, que é oxidado para dar o derivado manourônico.
O tratamento com ácido clorídrico transforma o derivado manourônico em diazocetona. O tratamento com diazobenzil fosfórico produz uma mistura de L-glicerol-7-fosfato e D-glicerol-7-fosfato.
Referências
- Collins, PM 2006. Dicionário de carboidratos com CD-ROM. Chapman & Hall / CRC, Boca Raton.
- Cui, SW 2005. Hidratos de carbono alimentares: química, propriedades físicas e aplicações. Imprensa CRC, Boca Raton.
- Ferrier, RJ 2000. Química dos carboidratos: monossacarídeos, dissacarídeos e oligossacarídeos específicos. Sociedade Real de Química, Cambridge.
- Hofstad, T. 1974. A distribuição de heptose e 2-ceto-3-desoxi-octonato em Bacteroidaceae. Journal of General Microbiology, 85, 314–320
- Kosma, P. 2008. Ocorrência, síntese e biossíntese de heptoses bacterianas. Current Organic Chemistry, 12, 1021-1039.
- Nelson, DL, Cox, MM 2017. Princípios de Lehninger da bioquímica. WH Freeman, Nova Iorque.
- Pigman, W. 1957. Os carboidratos: química, bioquímica, fisiologia. Academic Press, Nova Iorque.
- Pigman, W., Horton, D. 1970. Os carboidratos: química e bioquímica. Academic Press, Nova Iorque.
- Sinnott, ML 2007. Estrutura e mecanismo de química e bioquímica de carboidratos. Sociedade Real de Química, Cambridge.
- Stick, RV, Williams, SJ 2009. Carboidratos: as moléculas essenciais da vida. Elsevier, Amsterdã.
- Voet, D., Voet, JG, Pratt, CW 2008. Fundamentos da bioquímica – vida no nível molecular. Wiley, Hoboken.