Uma solução hipotônica é uma solução que possui uma concentração de solutos menor do que a concentração de solutos dentro de uma célula. Isso significa que a quantidade de solutos fora da célula é menor do que a quantidade de solutos dentro da célula, levando a um aumento no volume da célula devido à entrada de água por osmose.
Para preparar uma solução hipotônica, basta diluir uma quantidade menor de solutos em uma quantidade maior de solvente. Por exemplo, dissolver menos sal em mais água para criar uma solução hipotônica de sal.
Exemplos de soluções hipotônicas incluem água destilada, solução de glicose diluída e solução de soro fisiológico diluída. Essas soluções são comumente utilizadas em processos de osmose em células vivas, como na preservação de órgãos para transplantes e na administração de fluidos intravenosos.
Conheça as possíveis soluções hipotônicas para os seus problemas de saúde.
As soluções hipotônicas são uma ótima opção para tratar diversos problemas de saúde de forma natural e eficaz. Essas soluções possuem uma concentração de solutos menor que a do meio intracelular, o que ajuda a reequilibrar o gradiente osmótico das células.
Para preparar uma solução hipotônica, basta misturar água destilada com uma pequena quantidade de soluto, como sal ou glicose. É importante seguir as instruções corretamente para garantir a eficácia do tratamento.
Alguns exemplos de soluções hipotônicas incluem soro fisiológico, água destilada e soluções de glicose a baixa concentração. Essas soluções são utilizadas em diversos contextos, como na reidratação de pacientes desidratados, na limpeza de feridas e na irrigação de mucosas.
Portanto, se você está em busca de uma alternativa natural e segura para tratar seus problemas de saúde, considere utilizar soluções hipotônicas. Consulte um profissional de saúde para receber orientações específicas e descubra os benefícios que essas soluções podem oferecer para o seu bem-estar.
Quando é apropriado utilizar solução hipotônica para tratamentos específicos em saúde.
Quando se trata de tratamentos de saúde, a escolha da solução correta é essencial para garantir a eficácia do tratamento. Uma opção que pode ser utilizada em determinadas situações é a solução hipotônica. Mas afinal, quando é apropriado utilizar solução hipotônica para tratamentos específicos em saúde?
Antes de mais nada, é importante entender o que é uma solução hipotônica. Uma solução hipotônica é aquela que possui uma concentração de solutos menor do que a concentração de solutos dentro das células do corpo. Isso significa que, ao ser administrada, a solução hipotônica irá resultar em um fluxo de água para dentro das células, levando a uma possível expansão celular.
Um dos principais usos da solução hipotônica na área da saúde é para reidratação de pacientes desidratados. Em casos de desidratação severa, a solução hipotônica pode ser utilizada para repor os fluidos perdidos e restabelecer o equilíbrio hídrico no organismo.
Além disso, a solução hipotônica também pode ser utilizada para irrigação de feridas, pois ajuda a limpar a área afetada e promover a cicatrização. Nesses casos, a solução hipotônica é capaz de remover as impurezas e auxiliar no processo de regeneração dos tecidos.
No entanto, é sempre importante consultar um profissional de saúde para determinar a melhor abordagem terapêutica para cada situação.
Exemplo de solução isotônica: compreendendo sua importância na fisiologia celular e humana.
Uma solução isotônica é aquela em que a concentração de solutos é a mesma dentro e fora da célula. Isso significa que não haverá movimentação de água através da membrana celular, mantendo assim o equilíbrio osmótico. Um exemplo comum de solução isotônica é a solução salina a 0,9%, que é frequentemente utilizada em procedimentos médicos.
A importância da solução isotônica na fisiologia celular e humana está relacionada à manutenção do equilíbrio osmótico das células. Quando uma célula é exposta a uma solução hipotônica, por exemplo, ocorre um influxo de água para dentro da célula, levando ao inchaço e possivelmente à ruptura da célula. Por outro lado, em uma solução hipertônica, há um efluxo de água da célula, levando à desidratação e possível morte celular.
Portanto, a utilização de soluções isotônicas é fundamental em diversos processos biológicos, como a administração de fluidos intravenosos, a preservação de órgãos para transplantes e até mesmo na fabricação de medicamentos. Ao garantir que as células mantenham seu equilíbrio osmótico, as soluções isotônicas ajudam a manter a homeostase do organismo e garantir seu bom funcionamento.
Quando uma solução apresenta menor concentração de solutos em relação ao meio externo.
Uma solução é considerada hipotônica quando a concentração de solutos dentro dela é menor em comparação com o meio externo. Isso significa que a quantidade de partículas dissolvidas na solução é menor do que a quantidade de partículas presentes fora dela.
Para preparar uma solução hipotônica, é necessário diluir uma quantidade específica de soluto em uma quantidade maior de solvente. Isso resultará em uma solução com menor concentração de solutos em relação ao meio externo.
Um exemplo comum de solução hipotônica é a água pura. Quando comparada com o meio externo, que pode conter sais e outras substâncias dissolvidas, a água pura apresenta uma concentração de solutos menor.
Solução hipotônica: componentes, preparação, exemplos
Uma solução hipotônica é aquela que possui uma concentração mais baixa de soluto em comparação com uma solução separada ou isolada por uma barreira semipermeável. Essa barreira permite que o solvente passe por ela, água no caso de sistemas biológicos, mas nem todas as partículas de soluto.
Os fluidos corporais dos vertebrados intracelulares e extracelulares têm uma osmolaridade de cerca de 300 mOsm / L. Enquanto um líquido hipotônico é considerado com osmolaridade menor que 280 mOsm / L. Portanto, uma solução dessa osmolaridade é hipotônica em relação ao ambiente celular.
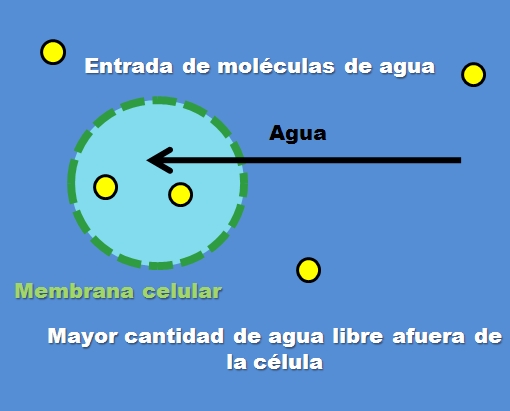
Um exemplo de uma solução hipotônica é 0,45% de cloreto de sódio. Mas como a célula ou o compartimento se comporta contra esse tipo de solução? A imagem acima responde a esta pergunta.
A concentração de partículas de soluto (pontos amarelos) é maior dentro da célula do que fora. Como há menos soluto ao redor da célula, há mais moléculas de água livre, portanto é representada com uma cor azul mais intensa em comparação com o interior da célula.
A água flui de fora para dentro através de osmose para nivelar as concentrações. Como resultado, a célula se expande ou incha absorvendo a água que passa através de sua membrana celular.
Componentes de soluções hipotônicas
As soluções hipotônicas consistem em um solvente que, salvo indicação em contrário, consiste em água e solutos nele dissolvidos, como sais, açúcares, etc., na forma pura ou mista. Mas essa solução não terá tonicidade se não houver barreira semi-permeável envolvida, que é a membrana celular.
Deve haver poucos sais dissolvidos para que sua concentração seja pequena, enquanto a “concentração” da água é alta. Como há mais água livre fora da célula, ou seja, não são solventes ou hidratantes, maior a pressão sobre a membrana celular e mais ela tenderá a atravessá-la para diluir o fluido intracelular.
Preparação de uma solução hipotônica
Para a preparação dessas soluções, é seguido o mesmo protocolo que o seguido para outras soluções. Cálculos apropriados da massa dos solutos são feitos. Estes são pesados, dissolvidos em água e levados para um balão volumétrico no volume correspondente.
A solução hipotônica apresenta baixa osmolaridade, geralmente inferior a 280 mOsm / L. Portanto, ao preparar uma solução hipotônica, devemos calcular sua osmolaridade de forma que seu valor seja inferior a 280 mOsm / L. A osmolaridade pode ser calculada com a seguinte equação:
Osmolaridade = m · v · g
Onde m é a molaridade do soluto e v é o número de partículas nas quais um composto em solução se dissocia. Substâncias não eletrolíticas não se dissociam, portanto o valor de v é igual a 1. Este é o caso da glicose e de outros açúcares.
Enquanto g é o coeficiente osmótico. Este é um fator de correção para a interação de partículas (íons) eletricamente carregadas na solução. Para soluções diluídas e substâncias não dissociáveis, por exemplo, e novamente glicose, um valor de g é considerado igual a 1. A molaridade é então considerada idêntica à sua osmolaridade.
Exemplo 1
Prepare uma solução de cloreto de sódio (NaCl) a 0,5% (p / v), verificando se é ou não uma solução hipotônica. Peso molecular de NaCl = 58,5 g / mol.
Traga a solução de NaCl a 0,5% para um grama por litro:
NaCl em g / l = (0,5 g ÷ 100 mL) · 1.000 mL
= 5 g / L
E procedemos ao cálculo de sua molaridade para determinar posteriormente sua osmolaridade:
Molaridade = massa (g / L) weight peso molecular (g / mol)
= 5 g / L ÷ 58,5 g / mol
= 0,085 moles / L
O NaCl se dissocia em duas partículas: Na + (cátion) e Cl – (ânion). Portanto, o valor de v = 2. Além disso, como é uma solução diluída de NaCl a 0,5%, pode-se assumir que o valor de g (coeficiente osmótico) é 1. Temos então:
Osmolaridade (NaCl) = molaridade · v · g
= 0,085 M · 2 · 1
= 0,170 Osm / L ou 170 mOsm / L
Esta é uma solução hipotônica, pois sua osmolaridade é muito menor que a osmolaridade de referência para fluidos corporais, que é a osmolaridade plasmática cujo valor é de cerca de 300 mOsm / L.
Exemplo 2
Prepare uma solução de uma mistura de cloreto de cálcio a 0,055% (p / v) (CaCl 2 ) e glicose a 4% (p / v) (C 6 H 12 O 6 ). Os pesos moleculares: CaCl 2 = 111 g / mol e C 6 H 12 O 6 = 180 g / mol.
Calculamos a molaridade com as concentrações dos respectivos solutos a 0,55 g / L e 40 g / L:
Molaridade (CaCl 2 ) = 0,55 g / L ÷ 111 g / mol
= 4,95 · 10 -3 M
= 4,95 mM
Molaridade (C 6 H 12 O 6 ) = 40 g / L ÷ 180 g / mol
= 0,222 M
= 222 mM
E da mesma forma calculamos as osmolaridades, sabendo que o CaCl 2 se dissocia em três íons, dois Cl – e um Ca 2+ , e assumindo que sejam soluções muito diluídas, então o valor de v é 1. Temos então :
Osmolaridade (CaCl 2 ) = 4,95 mM · 3 · 1
= 14,85 mOsm / L
Osmolaridade de (C 6 H 12 O 6 ) = 222 mM · 1 · 1
= 222 mOsm / L
Finalmente, a osmolaridade total da solução se torna a soma das osmolaridades individuais; isto é, daqueles de NaCl e glicose. Isto é, portanto:
Osmolaridade total da solução = osmolaridade de CaCl 2 + osmolaridade C 6 H 12 O 6
= 222 mOsm / L + 14,85 mOsm / L
= 236,85 mOsm / L
A solução da mistura de glicose com cloreto de cálcio é hipotônica, pois sua osmolaridade (236,85 mOsm / L) é muito menor que a osmolaridade plasmática (300 mOsm / L), que é tomada como referência.
Exemplos de soluções hipotônicas
Solução de cloreto de sódio
A solução de cloreto de sódio a 0,45% (NaCl) é administrada por via intravenosa a pacientes com cetose diabética que desenvolvem desidratação nos compartimentos intersticial e intracelular. A água flui do plasma para esses compartimentos.
Solução de Ringer com lactato
A solução de lactato nº 19 da Ringer é outro exemplo de solução hipotônica. Sua composição é 0,6 g de cloreto de sódio, 0,03 g de cloreto de potássio, 0,02 g de cloreto de cálcio, 0,31 g de lactato de sódio e 100 mL de água destilada. É uma solução usada para a reidratação dos pacientes e é levemente hipotônica (274 mosm / L).
Referências
- De Lehr Spilva, A. e Muktans, Y. (1999). Guia de especialidades farmacêuticas na Venezuela . XXXVª Edição. Edições Globais.
- Whitten, Davis, Peck e Stanley. (2008). Chemistry . (8a ed.). Aprendizagem CENGAGE.
- Wikipedia. (2020). Tonicidade. Recuperado de: en.wikipedia.org
- Union Media LLC. (2020). Soluções isotônicas, hipotônicas e hipertônicas. Recuperado de: uniontestprep.com
- Lodish H., Berk A., Zipursky SL, et al. (2000) Seção 15.8 Osmose, canais de água e regulação do volume celular. Estante NCBI. Recuperado de: ncbi.nlm.nih.gov
- John Brennan. (13 de março de 2018). Como calcular a isotonicidade. Recuperado de: sciencing.com