O triptofano é um aminoácido essencial para o corpo humano e desempenha diversas funções importantes no organismo. Sua estrutura química é fundamental para a produção de serotonina, um neurotransmissor responsável pela regulação do humor, sono, apetite e até mesmo da cognição. Além disso, o triptofano é essencial para a síntese de melatonina, um hormônio que regula o ciclo de sono e vigília. Por esses motivos, o triptofano é conhecido por seus benefícios para a saúde mental, auxiliando no combate à depressão, ansiedade e insônia, além de contribuir para o bom funcionamento do sistema imunológico e a regulação do apetite.
Principais características do triptofano e sua importância para o corpo humano.
O triptofano é um aminoácido essencial que desempenha um papel fundamental no corpo humano. Sua estrutura química inclui um grupo amino e um anel aromático, sendo precursor da serotonina, melatonina e niacina.
Este aminoácido não é produzido pelo organismo, sendo necessário adquiri-lo através da alimentação. Alimentos ricos em triptofano incluem carnes, peixes, ovos, nozes e sementes.
O triptofano é conhecido por sua capacidade de promover a sensação de bem-estar e relaxamento. Ele atua como um precursor da serotonina, neurotransmissor responsável pela regulação do humor, sono e apetite.
Além disso, o triptofano é essencial para a produção de melatonina, hormônio que regula o ciclo sono-vigília. Portanto, sua ingestão adequada pode contribuir para a qualidade do sono e redução do estresse.
Outro benefício do triptofano é sua importância na síntese de niacina, uma vitamina do complexo B essencial para o metabolismo energético e a saúde da pele, cabelos e sistema nervoso.
Sua ingestão adequada através da alimentação é fundamental para garantir o bem-estar e o bom funcionamento do corpo.
Importância do triptofano para o corpo humano: conheça a função desse aminoácido essencial.
O triptofano é um aminoácido essencial para o corpo humano, o que significa que ele não pode ser produzido pelo organismo e, portanto, deve ser obtido através da alimentação. Este aminoácido desempenha diversas funções importantes no nosso corpo, sendo fundamental para a síntese de proteínas e para a produção de neurotransmissores, como a serotonina.
O triptofano possui uma estrutura química específica que o torna essencial para a saúde e o bem-estar. Ele é um precursor da serotonina, um neurotransmissor responsável pela regulação do humor, do sono e do apetite. Por isso, a deficiência de triptofano pode estar relacionada a distúrbios como depressão, ansiedade e insônia.
Além disso, o triptofano também é importante para a regulação do sistema imunológico, contribuindo para a produção de anticorpos e para a resposta inflamatória do organismo. Ele também é essencial para a saúde da pele, dos cabelos e das unhas, sendo um componente importante na produção de colágeno.
Por fim, o triptofano também pode trazer benefícios para a saúde cardiovascular, ajudando a regular a pressão arterial e os níveis de colesterol no sangue. Sua presença na dieta é fundamental para garantir o bom funcionamento do organismo e prevenir uma série de problemas de saúde.
Benefícios e indicações do uso do remédio tryptophan para o organismo humano.
O Triptofano é um aminoácido essencial para o organismo humano, o qual não pode ser produzido pelo corpo e, portanto, deve ser obtido por meio da alimentação ou suplementação. Sua estrutura química inclui um grupo amina e um grupo carboxila, sendo precursor da serotonina, melatonina e niacina.
Este aminoácido desempenha diversas funções no organismo, sendo fundamental para a regulação do humor, sono e apetite. Além disso, o Triptofano também contribui para a síntese de proteínas, regulação do sistema imunológico e produção de neurotransmissores.
Alguns dos benefícios do uso do Triptofano para o organismo humano incluem a melhoria do humor, redução da ansiedade e do estresse, regulação do sono, aumento da sensação de bem-estar e melhora da concentração e memória. Indicações para o uso do Triptofano incluem casos de depressão, insônia, ansiedade, transtornos alimentares e déficit de atenção.
Portanto, o uso do Triptofano como suplemento pode trazer diversos benefícios para a saúde mental e física, ajudando a promover o equilíbrio emocional e o bem-estar geral. Consulte sempre um profissional de saúde antes de iniciar qualquer tipo de suplementação com Triptofano.
Conheça os diferentes tipos de triptofano e suas funções no organismo humano.
O triptofano é um aminoácido essencial que desempenha um papel fundamental no organismo humano. Ele é conhecido por ser o precursor da serotonina, um neurotransmissor que regula o humor, o sono e o apetite. Além disso, o triptofano também é convertido em niacina, uma vitamina do complexo B que desempenha diversas funções no organismo.
Existem dois tipos de triptofano: o L-triptofano e o D-triptofano. O L-triptofano é o tipo mais comum e é encontrado em alimentos como carne, peixe, ovos e laticínios. Já o D-triptofano é menos comum e é encontrado em algumas plantas e bactérias.
O triptofano tem diversos benefícios para a saúde. Ele ajuda a regular o sono, melhorar o humor, reduzir a ansiedade e o estresse, além de promover o bem-estar geral. Além disso, o triptofano também é importante para a síntese de proteínas no organismo.
É importante garantir a sua ingestão adequada através da alimentação ou suplementação, para manter a saúde e o bem-estar em dia.
Triptofano: características, estrutura, funções, benefícios
O triptofano (Trp, W) é classificado dentro do grupo dos aminoácidos essenciais de aminoácidos porque o corpo humano não pode sintetizar e deve obter -lo através da dieta.
Alguns alimentos, como leite e seus derivados, carnes, ovos e alguns cereais, como quinoa e soja, contêm aminoácidos essenciais e, portanto, são uma importante fonte de triptofano.
Na natureza, mais de 300 aminoácidos diferentes são conhecidos e, destes, apenas 22 constituem as unidades monoméricas das proteínas celulares. Entre os últimos, 9 são aminoácidos essenciais, incluindo o triptofano, no entanto, a essencialidade de cada um difere entre as espécies.
O triptofano possui várias funções, incluindo sua participação na síntese de proteínas, na síntese de serotonina, que é um potente vasoconstritor e neurotransmissor, na melatonina e na síntese do cofator NAD.
No reino vegetal, o triptofano é um precursor fundamental do hormônio vegetal conhecido como auxina (ácido indol-3-acético). Ele pode ser sintetizado por algumas bactérias, como E. coli, do corismato, que é produzido a partir de alguns derivados glicolíticos, como fosfoenolpiruvato e eritrose-4-fosfato.
Sua degradação em mamíferos ocorre no fígado, onde é utilizado para a síntese da acetil coenzima A (acetil-CoA) e, por esse motivo, é descrito como um aminoácido chamado glicogênico, pois pode entrar no ciclo de formação da glicose.
Vários estudos foram relatados com resultados controversos relacionados ao uso do triptofano como complemento alimentar para o tratamento de algumas patologias, como depressão e alguns distúrbios do sono, entre outros.
Existem algumas doenças relacionadas a defeitos congênitos no metabolismo de aminoácidos. No caso do triptofano, a doença de Hartnup pode ser denominada, devido a uma deficiência de triptofano-2,3-monooxigenase, uma doença hereditária recessiva caracterizada por retardo mental e distúrbios da pele semelhantes à pelagra.
Caracteristicas
Juntamente com a fenilalanina e a tirosina, o triptofano faz parte do grupo de aminoácidos aromáticos e hidrofóbicos.
No entanto, o triptofano é caracterizado por ser um aminoácido levemente hidrofóbico, pois sua cadeia lateral aromática, possuindo grupos polares, atenua essa hidrofobicidade.
Por possuírem anéis conjugados, possuem uma forte absorção de luz na região do espectro ultravioleta próximo e essa característica é frequentemente usada para a análise estrutural de proteínas.
Absorve a luz ultravioleta (entre 250 e 290 nm) e, embora esse aminoácido não seja muito abundante na estrutura da maioria das proteínas do corpo humano, sua presença representa uma importante contribuição para a capacidade de absorção da luz no organismo. Região de 280 nm da maioria das proteínas.
Os requisitos diários de triptofano diferem com a idade. Em bebês entre 4 e 6 meses, a exigência média é de cerca de 17 mg por quilograma de peso por dia; em crianças de 10 a 12 anos, é de 3,3 mg por quilograma de peso por dia e em adultos é de 3,5 mg por quilograma de peso por dia.
O triptofano é absorvido pela via intestinal e é um aminoácido cetogênico e glicogênico ao mesmo tempo.
Por ser um precursor da serotonina, um importante neurotransmissor, o triptofano deve atingir o sistema nervoso central (SNC) e, para isso, deve atravessar a barreira hematoencefálica, para a qual existe um mecanismo de transporte ativo específico.
Estrutura
O triptofano possui uma fórmula molecular C11H12N2O2 e esse aminoácido essencial possui uma cadeia lateral aromática.
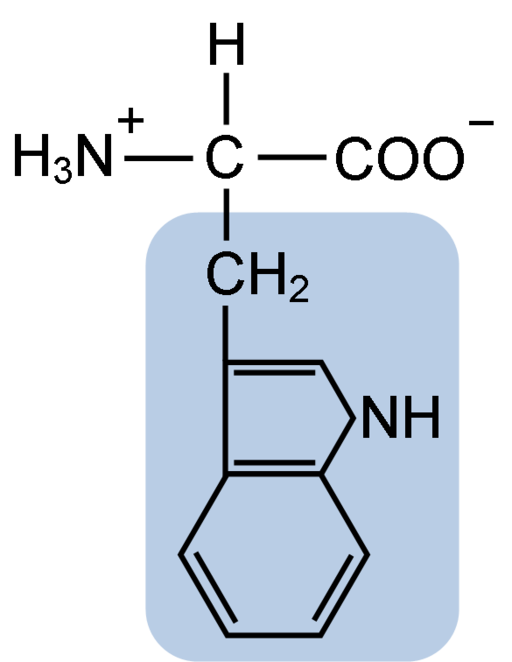
Como todos os aminoácidos, o triptofano possui um átomo de carbono α ligado a um grupo amino (NH2), um átomo de hidrogênio (H), um grupo carboxila (COOH) e uma cadeia lateral (R) formada por uma estrutura heterocíclica, o grupo indole
Seu nome químico é ácido 2-amino-3-indolilpropiônico, possui uma massa molecular de 204,23 g / mol. A sua solubilidade a 20 ° C é de 1,06 g em 100 g de água e tem uma densidade de 1,34 g / cm3.
Funções
Nos seres humanos, o triptofano é usado para a síntese de proteínas e é essencial para a formação da serotonina (5-hidroxitriptamina), um vasoconstritor potente, estimulando a contração da musculatura lisa (especialmente no intestino delgado) e um neurotransmissor capaz de gerar estimulação psíquica, combater a depressão e regular a ansiedade.
O triptofano é um precursor na síntese de melatonina e, portanto, tem implicações nos ciclos de sono e vigília.
O referido aminoácido é usado como precursor em uma das três vias para a formação do cofator NAD, um cofator muito importante que participa de uma ampla variedade de reações enzimáticas relacionadas a eventos de redução de óxidos.
O triptofano e alguns de seus precursores são usados para formar um hormônio vegetal chamado auxina (ácido indol-3-acético). Auxinas são hormônios vegetais que regulam o crescimento, desenvolvimento e muitas outras funções fisiológicas das plantas.
Biossíntese
Em organismos capazes de sintetizá-lo, o esqueleto de carbono do triptofano é derivado do fosfoenolpiruvato e eritrose-4-fosfato. Estes, por sua vez, são formados a partir de um intermediário do ciclo de Krebs: o oxaloacetato.
Fosfoenolpiruvato e eritrose-4-fosfato são usados para a síntese de corismato em uma rota de sete etapas enzimáticas. O fosfoenolpiruvato (PEP) é um produto da glicólise e eritrose-4-fosfato da via da pentose fosfato.
Como é o caminho de síntese do corismato?
O primeiro passo na síntese do corismato é a união da PEP com eritrose-4-fosfato para formar 2-ceto-3-desoxi-D-arabino-heptulosonato-7-fosfato (DAHP).
Essa reação é catalisada pela enzima 2-ceto-3-desoxi-D-arabino-heptulosonato-7-fosfato sintase (DAHP sintase), que é inibida pelo crismato.
A segunda reação envolve a ciclização de DAHP pela desidrocinato sintase, uma enzima que requer o cofator NAD, que é reduzido durante essa reação; como resultado, é produzido o 5-desidroquinato.
O terceiro passo dessa rota envolve a remoção de uma molécula de água 5-desidroquinato, uma reação catalisada pela enzima desidroquinato desidratase, cujo produto final corresponde ao 5-desidro hidroquímico.
O grupo ceto desta molécula é reduzido a um grupo hidroxila e, como conseqüência, o shikimato é formado. A enzima que catalisa essa reação é a shikimato desidrogenase dependente de NADPH.
O quinto passo da rota envolve a formação do shikimato 5-fosfato e o consumo de uma molécula de ATP por uma enzima conhecida como shikimato quinase, responsável pela fosforilação do shikimato na posição 5.
Posteriormente, a partir do shiquimato de 5-fosfato e pela ação da 3-enolpiruvil shikimato-5-fosfato sintase, é gerado o shikimato de 3-enolpiruvil 5-fosfato. A enzima acima mencionada promove o deslocamento do grupo fosforil de uma segunda molécula de PEP pelo grupo hidroxila do carbono na posição 5 do shiquimato de 5-fosfato.
A sétima e última reação é catalisada pela corismato sintase, que remove o fosfato de 3-enolpiruvil shikimato 5-fosfato e o converte em corismato.
No fungo N. crassa , um único complexo enzimático multifuncional catalisa cinco das sete reações dessa via e, para esse complexo, existem outras três enzimas que acabam gerando triptofano.
Síntese de triptofano em bactérias
Em E. coli, a transformação do corismato em triptofano inclui uma rota de cinco etapas enzimáticas adicionais:
Primeiro, a enzima antranilato sintase converte o corismato em antranilato. Uma molécula de glutamina participa dessa reação, que doa o grupo amino que se liga ao anel indol do triptofano e se torna glutamato.
O segundo passo é catalisado pelo antranilato de fosforibosil transferase. Nesta reação, uma molécula de pirofosfato de 5-fosforibibosil-1-pirofosfato (PRPP) é deslocada, um metabólito rico em energia e um N- (5′-fosforibosil) -antranilato é formado.
A terceira reação dessa rota de síntese do triptofano envolve a participação da enzima fosforibosil antranilato isomerase. Aqui, o anel furano do N- (5′-fosforibosil) -antranilato é aberto e o 5-fosfato de 1- (o-carboxifenilamino) -1-desoxiribulose é formado por tautomerização.
Além disso, o fosfato de indol-3-glicerol é formado, em uma reação catalisada pela indol-3-glicerol-fosfato sintase, onde o CO2 e uma molécula de H2O são liberados e o 1- (o-carboxifenilamino) -1- é ciclado Desoxirribulose 5-fosfato.
A última reação dessa via acaba formando triptofano quando o triptofano sintase catalisa a reação do fosfato de indol-3-glicerol com uma molécula de PLP (fosfato de piridoxal) e outra de serina, liberando o gliceraldeído 3-fosfato e formando o triptofano.
Degradação
Nos mamíferos, o triptofano é degradado no fígado para acetil-CoA, em uma rota que envolve doze etapas enzimáticas: oito para atingir α-cetoadipato e 4 outras para converter α-cetoadipato em acetil coenzima A.
A ordem de degradação do α-cetoadipato é:
Triptofano → N- formil quinurenina → Quinurenina → 3-hidroxi quinurenina → 3-hidroxi-antranilato → ε-semialdeído 2-amino-3-carboxi-mucônico → ε-semialdeído α-amino mucônico → 2-amino muconato → α-cetoadipato.
As enzimas que catalisam essas reações, respectivamente, são:
Triptofano 2-3-dioxigenase, quinurenina formamidase, monooxigenase dependente de NADPH, quinureninase, 3-hidroxi-antranilato oxigenase, descarboxilase, ε-semialdeído desidrogenase α-aminonucônico desidrogenase dependente de NAD e α-amino muconato redutase Dependente de NADPH.
Uma vez gerado o α-cetoadipato, o glutaril-CoA é formado por descarboxilação oxidativa. Por meio da oxidação β, forma-se Glutaconil-CoA que perde um átomo de carbono na forma de bicarbonato (HCO3-), ganha uma molécula de água e acaba como crotonil-CoA.
Crotonil-CoA, também por β-oxidação, produz acetil-CoA. O referido acetil-CoA pode seguir várias rotas entre as quais se destaca a gliconeogênese, para formar glicose e o ciclo de Krebs, para formar ATP, conforme necessário.
No entanto, essa molécula também pode ser direcionada para a formação de corpos cetônicos, que podem finalmente ser usados como fonte de energia.
Alimentos ricos em triptofano
Carne vermelha em geral, frango e peixe (especialmente peixes azuis como salmão e atum) são especialmente ricos em triptofano. O leite e seus derivados, ovos, especialmente a gema, também são alimentos com abundante teor de triptofano.
Outros alimentos que servem como fonte natural desse aminoácido são:
– Nozes como nozes, amêndoas, pistache e castanha de caju, entre outras.
– Cereais de arroz.
– Grãos secos, como feijão, lentilha, grão de bico, soja, quinoa, etc.
– Levedura de cerveja e feijão fresco, banana e banana, abacaxi ou abacaxi, abacate, ameixa, agrião, brócolis, espinafre e chocolate.
Benefícios da sua ingestão
O consumo de triptofano é absolutamente necessário para sintetizar todas as proteínas que o incluem em sua estrutura e, por meio de suas diferentes funções, permite regular os ciclos de humor, sono e vigília e uma ampla variedade de processos bioquímicos nos quais a NAD participa .
Além dos efeitos conhecidos sobre o humor, a serotonina (derivada do triptofano) está envolvida em múltiplas funções cognitivas relacionadas ao aprendizado e à memória que, portanto, também se relacionam ao triptofano.
Existem dados que mostram a relação entre humor, serotonina e o eixo gastrointestinal-cerebral como um sistema de influências bidirecionais entre os centros emocionais e cognitivos do cérebro e a função periférica do trato digestivo.
O uso como complemento alimentar para o tratamento de alguns distúrbios, principalmente os relacionados ao sistema nervoso central, tem sido bastante controverso, pois seu transporte competitivo com aminoácidos neutros, muito mais abundantes, dificulta a obtenção de aumentos significativos e sustentados de Triptofano após administração oral.
Apesar dessas controvérsias, seu uso como adjuvante em:
– Tratamento da dor
– Transtornos do sono
– Tratamento de depressão
– Tratamento de manias
– Redução de apetite
Distúrbios de deficiência
A eliminação ou falta central de triptofano é acompanhada por depressão, falhas na atenção, diminuição da memória, distúrbios do sono e ansiedade.
Em pacientes deprimidos com tendências suicidas, foram encontradas alterações na concentração de sangue de triptofano e líquido cefalorraquidiano. Além disso, alguns pacientes com anorexia nervosa apresentam baixos níveis séricos de triptofano.
Alguns pacientes poliúricos, que perdem vitamina B6 e zinco, freqüentemente apresentam fobias e ansiedade e melhoram com suplementos alimentares ricos em triptofano.
A síndrome carcinóide é caracterizada pela presença de tumores no intestino delgado que causam diarréia, doenças vasculares e broncoconstrição e está relacionada à deficiência de niacina e triptofano.
A pelagra é uma condição patológica que é acompanhada por diarréia, demência, dermatite e pode causar a morte. Também é tratada com suplementos de niacina e triptofano.
A doença de Hartnup tem a ver, entre algumas coisas, com um defeito no metabolismo de vários aminoácidos, incluindo o triptofano.
No caso da deficiência da enzima triptofano-2,3-monooxigenase, essa é uma doença hereditária recessiva caracterizada por retardo mental e distúrbios da pele semelhantes à pelagra.
Referências
- Halvorsen, K. & Halvorsen, S. (1963). Doença de Hartnup Pediatrics , 31 (1), 29-38.
- Hood, SD, Bell, CJ, Argyropoulos, SV e Nutt, DJ (2016). Não entre em pânico Um guia para a depleção do triptofano com provocação de ansiedade específica para um distúrbio. Journal of Psychopharmacology , 30 (11), 1137-1140.
- Jenkins, TA, Nguyen, JC, Polglaze, KE e Bertrand, PP (2016). Influência do triptofano e da serotonina no humor e na cognição com um possível papel do eixo intestino-cérebro. Nutrientes , 8 (1), 56.
- Os dados foram analisados por meio de entrevistas semiestruturadas e entrevistas semiestruturadas. Efeitos ansiolíticos da depleção aguda de triptofano na anorexia nervosa. International Journal of Eating Disorders , 33 (3), 257-267.
- Murray, RK, Granner, DK, Mayes, P., & Rodwell, V. (2009). Bioquímica ilustrada de Harper. 28 (p. 588). Nova York: McGraw-Hill.
- Nelson, DL, Lehninger, AL, & Cox, MM (2008). Princípios de Lehninger da bioquímica . Macmillan