A troponina é uma proteína muscular que desempenha um papel crucial na contração do músculo cardíaco. Ela é composta por três subunidades: troponina C, troponina I e troponina T. A troponina I é específica para o músculo cardíaco e é liberada na corrente sanguínea quando há lesão ou morte das células do músculo cardíaco. Por isso, o teste de troponina é amplamente utilizado como um marcador de lesão cardíaca, como o infarto do miocárdio. A detecção de níveis elevados de troponina no sangue indica a presença de danos ao músculo cardíaco e pode ajudar no diagnóstico e tratamento de doenças cardíacas.
Troponina: o que é e qual sua importância no funcionamento cardíaco do corpo humano.
Troponina: A troponina é uma proteína encontrada nas células musculares, principalmente no músculo cardíaco. Ela desempenha um papel fundamental na contração muscular e é essencial para o funcionamento adequado do coração.
Características: A troponina é composta por três subunidades – troponina C, troponina I e troponina T. Cada uma dessas subunidades desempenha um papel específico na regulação da contração muscular, garantindo que o coração funcione de maneira eficiente.
Estrutura: A troponina é uma proteína filamentosa que se liga ao cálcio, desencadeando a contração muscular. Sua estrutura complexa permite que ela interaja com outros componentes do músculo cardíaco, garantindo a sincronia necessária para o bombeamento de sangue pelo coração.
Funções: A troponina regula a interação entre actina e miosina, dois filamentos que compõem as células musculares. Quando o coração recebe um estímulo para se contrair, a troponina atua como um interruptor molecular, permitindo que a contração ocorra de maneira coordenada.
Teste: O teste de troponina é frequentemente utilizado para diagnosticar danos no músculo cardíaco, como um ataque cardíaco. A presença de troponina no sangue indica que houve lesão nas células do coração, permitindo aos médicos identificar e tratar problemas cardíacos de forma rápida e eficaz.
Em resumo, a troponina é uma proteína essencial para o funcionamento cardíaco, garantindo a contração adequada do músculo do coração. Seu papel na regulação da contração muscular a torna uma ferramenta importante no diagnóstico de doenças cardíacas, permitindo intervenções precoces e salvando vidas.
Entenda o procedimento do teste de troponina e sua relevância para diagnóstico cardíaco.
O teste de troponina é um exame de sangue utilizado para detectar a presença da proteína troponina, que é liberada nas células do coração quando há lesão no músculo cardíaco. Este teste é fundamental para o diagnóstico de eventos cardíacos agudos, como o infarto do miocárdio.
A troponina é uma proteína complexa composta por três subunidades: troponina C, troponina I e troponina T. Estas subunidades desempenham um papel crucial na contração muscular do coração, regulando a interação entre a actina e a miosina.
Para realizar o teste de troponina, uma amostra de sangue é coletada e analisada em laboratório. A presença elevada de troponina no sangue indica lesão no músculo cardíaco, pois esta proteína é específica do coração e não é encontrada em outros tecidos.
A relevância do teste de troponina no diagnóstico cardíaco reside no fato de que ele é altamente sensível e específico para detectar lesões no músculo cardíaco. Isso permite aos médicos identificar rapidamente a ocorrência de um infarto do miocárdio e iniciar o tratamento adequado, reduzindo assim o risco de complicações e danos permanentes no coração.
Em resumo, o teste de troponina é uma ferramenta essencial no diagnóstico de eventos cardíacos agudos, fornecendo informações precisas e confiáveis sobre a saúde do músculo cardíaco. Portanto, é importante realizar este exame sempre que houver suspeita de problemas cardíacos, para garantir um diagnóstico precoce e um tratamento eficaz.
Importância da troponina na ativação da contração dos músculos esqueléticos e cardíacos.
A troponina é uma proteína essencial para a contração dos músculos esqueléticos e cardíacos. Ela atua regulando a interação entre a actina e a miosina, o que permite a contração muscular. A troponina é composta por três subunidades: troponina C, troponina I e troponina T.
A subunidade troponina C possui sítios de ligação ao cálcio, que é crucial para a ativação da contração muscular. Quando o cálcio se liga à troponina C, ocorre uma mudança conformacional na troponina, que permite a interação entre a actina e a miosina. Isso resulta na contração muscular.
A subunidade troponina I inibe a interação entre a actina e a miosina na ausência de cálcio, garantindo que a contração muscular seja controlada e ocorra apenas quando necessário. Já a subunidade troponina T se liga à tropomiosina, ajudando a regular a interação entre a actina e a miosina.
O teste de troponina é frequentemente utilizado para diagnosticar lesões cardíacas, uma vez que a troponina cardíaca é liberada na corrente sanguínea quando há dano ao músculo cardíaco. Portanto, a troponina desempenha um papel crucial não apenas na contração dos músculos, mas também no diagnóstico de condições cardíacas.
Qual é a localização da troponina no organismo humano?
A troponina é uma proteína que se encontra principalmente no miocárdio, o músculo do coração, e nos miócitos, as células musculares cardíacas. Ela desempenha um papel fundamental na contração muscular, sendo responsável por regular a interação entre a actina e a miosina, as proteínas contráteis presentes nos músculos.
Quando ocorre um dano ao músculo cardíaco, como no caso de um infarto do miocárdio, a troponina é liberada na corrente sanguínea. Por isso, a medição dos níveis de troponina no sangue é um exame importante para diagnosticar e avaliar a gravidade de lesões no coração.
Além do coração, a troponina também pode ser encontrada em menor quantidade em outros tipos de músculos esqueléticos, como o esquelético, mas a sua presença no miocárdio é mais significativa do ponto de vista clínico.
Troponina: características, estrutura, funções e teste
Troponina é o nome que recebe uma proteína presente no músculo esquelético e cardíaco dos vertebrados, associada aos filamentos nas fibras musculares e que tem funções na regulação da atividade contrátil (contração e relaxamento muscular).
As fibras musculares são as células que compõem o tecido muscular, cuja capacidade de contração é baseada na interação entre filamentos ordenados e intimamente associados no interior, ocupando a maior parte do volume citoplasmático.

Esses filamentos são conhecidos como miofilamentos e existem dois tipos: grosso e fino. Os filamentos grossos são compostos de moléculas de miosina II, enquanto os finos são polímeros de actina globular ou actina G em associação com outras duas proteínas.
Tanto a actina quanto a miosina também são encontradas em outras células do corpo humano e em outros organismos, apenas em proporção muito menor e participando de diferentes processos, como migração celular, exocitose, citocinesia (durante a divisão celular) e até tráfego vesicular intracelular.
Troponina e tropomiosina são as duas proteínas associadas aos filamentos finos de actina que participam na regulação dos processos de contração e relaxamento das miofibrilas das células ou fibras musculares.
Os mecanismos de ação pelos quais essas duas proteínas exercem sua função estão relacionados à concentração intracelular de cálcio. O sistema de regulação da troponina é um dos sistemas mais conhecidos na fisiologia e bioquímica da contração do músculo esquelético.
Essas proteínas são de grande importância para o organismo. Atualmente, sabe-se com certeza que algumas cardiomiopatias familiares ou congênitas são o resultado de mutações na sequência dos genes que codificam (troponina ou tropomiosina).
Caracteristicas
A troponina está associada à actina dos filamentos finos das fibras musculares do músculo esquelético e cardíaco, numa razão estequiométrica de 1 a 7, ou seja, uma molécula de troponina para cada 7 moléculas de actina.
Essa proteína, como observada, é encontrada exclusivamente nos filamentos contidos nas miofibrilas das fibras musculares estriadas esqueléticas e cardíacas, e não nas fibras musculares lisas que compõem a musculatura vascular e visceral.
É concebido por alguns autores como a proteína reguladora da tropomiosina. Assim, possui locais de ligação para interação com moléculas de actina, o que lhe confere a capacidade de regular sua interação com a miosina de filamentos espessos.
Nos miofilamentos, a proporção entre as moléculas de troponina e tropomiosina é de 1 para 1, o que significa que para cada complexo de troponina existente existe uma molécula de tropomiosina associada a ele.
Estrutura
A troponina é um complexo proteico composto por três subunidades globulares diferentes conhecidas como troponina I, troponina C e troponina T, que juntas somam cerca de 78 kDa.
No corpo humano, existem variantes específicas de tecido para cada uma dessas subunidades, que diferem entre si no nível genético e molecular (com relação aos genes que as codificam) e no nível estrutural (com relação às sequências de aminoácidos).
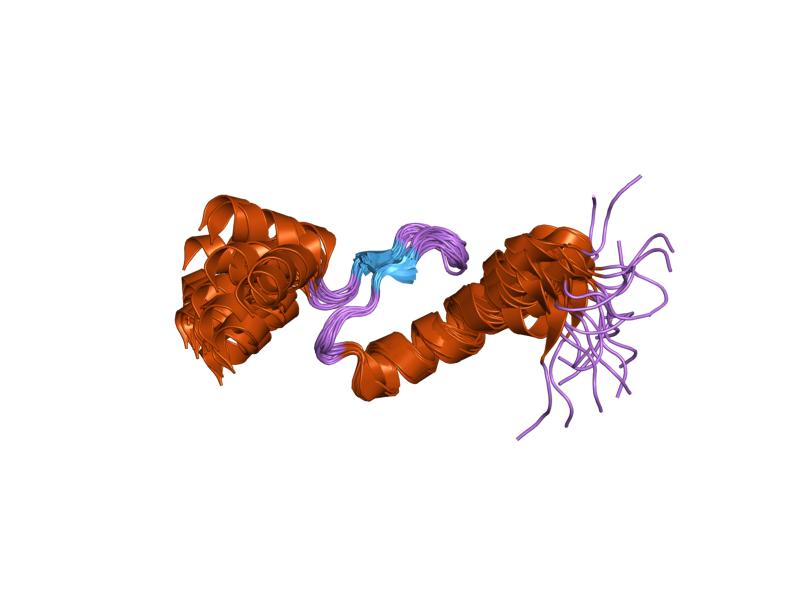
A troponina C ou TnC é a menor das três subunidades e talvez uma das mais importantes. Tem um peso molecular de 18 kDa e possui locais para ligar o cálcio (Ca2 +).
Troponina T ou TnT é a que possui os locais de ligação para ancorar o complexo das três subunidades à tropomiosina e possui 30 kDa de peso molecular; Também é conhecida como subunidade T ou subunidade de ligação à tropomiosina.
A troponina I ou TnI, com pouco mais de 180 resíduos de aminoácidos, tem o mesmo peso molecular da troponina T, mas em sua estrutura possui locais especiais para se ligar à actina, bloqueando a interação entre este e a miosina, que é o fenômeno responsável pela contração das fibras musculares.
Muitos livros didáticos se referem a essa subunidade como subunidade inibidora e “bastão” molecular entre as três subunidades da troponina. Sua capacidade de ligação à actina e sua atividade inibitória são aprimoradas por sua associação com a tropomiosina, mediada pela subunidade TnT.
Foi demonstrado que, na subunidade I, a região da sequência responsável pela inibição é definida por um peptídeo central de 12 resíduos de aminoácidos entre as posições 104 e 115; e que a região C-terminal da subunidade também tem uma função durante a inibição.
Funções
O principal papel da troponina na contração muscular depende de sua capacidade de se ligar ao cálcio, uma vez que essa proteína é o único componente dos filamentos finos no músculo estriado que possui essa propriedade.
Na ausência de troponina, os filamentos finos são capazes de se ligar a filamentos grossos e contrair-se, independentemente da concentração de cálcio intracelular, de modo que a função da troponina é impedir a contração na ausência de cálcio por sua associação à tropomiosina.
Assim, a troponina desempenha um papel importante na manutenção do relaxamento muscular quando não há cálcio intracelular suficiente e na contração muscular quando a estimulação elétrica do nervo permite que o cálcio entre na fibra muscular.
Como isso acontece?
Nos músculos estriados esqueléticos e cardíacos, a contração muscular ocorre graças à interação entre filamentos finos e grossos que deslizam um sobre o outro.
Nas células desses músculos, o cálcio é essencial para a interação ato-miosina (filamentos finos e grossos), uma vez que os locais de ligação da actina à miosina são “ocultos” pela ação conjunta da tropomiosina e troponina, que é a que responde ao cálcio.
Os íons de cálcio provenientes do retículo sarcoplasmático (o retículo endoplasmático das fibras musculares) se ligam à subunidade C da troponina, que neutraliza a inibição mediada pela troponina e desencadeia a contração muscular.
A “neutralização” da inibição causada pela subunidade I ocorre após a ligação do cálcio à subunidade C, que gera uma alteração conformacional que se propaga entre as três subunidades e permite sua dissociação das moléculas de actina e tropomiosina. .
Esta dissociação entre troponina, tropomiosina e actina expõe os locais de ligação da miosina na actina. É quando as cabeças globulares destas últimas podem interagir com as fibras de actina e iniciar a contração dependente de ATP, deslocando um filamento sobre o outro.
Teste de troponina
A troponina é o biomarcador preferido para a detecção de lesões cardíacas. Portanto, o teste da troponina é amplamente utilizado no diagnóstico bioquímico precoce e / ou preventivo de algumas condições patológicas cardíacas, como infarto agudo do miocárdio.
Muitos médicos responsáveis acreditam que esse teste facilita a tomada de decisões sobre o que fazer e qual tratamento dar aos pacientes com dor no peito.
Geralmente está relacionada à detecção das subunidades T e I da troponina, uma vez que a isoforma da troponina C também é encontrada nos músculos esqueléticos que se contraem lentamente; isto é, não é específico para o coração.
Em que se baseia o teste de troponina?
O teste da troponina é geralmente um teste imunológico que detecta as isoformas cardíacas das subunidades T e I da troponina. Então, é baseado nas diferenças que existem entre as duas isoformas.
Isoforma da subunidade troponina I (cTnI)
No tecido muscular do miocárdio, existe apenas uma isoforma da subunidade I da troponina, caracterizada pela presença de uma “cauda” pós-traducional de 32 aminoácidos em sua extremidade N-terminal.
Essa isoforma é detectada graças ao desenvolvimento de anticorpos monoclonais específicos que não reconhecem outras isoformas não cardíacas, uma vez que a cauda de aminoácidos é mais ou menos 50% diferente das extremidades de outras isoformas.
CTnI não é expresso em tecidos danificados, mas é exclusivo do tecido cardíaco adulto.
Isoforma da subunidade T da troponina T (cTnT)
A isoforma cardíaca da subunidade T da troponina é codificada em três genes diferentes, cujo RNAm pode sofrer emendas alternativas que resultam na produção de isoformas com sequências variáveis nas extremidades dos terminais N e C.
Embora o músculo cardíaco humano contenha 4 isoformas de TnT, apenas uma é característica do tecido cardíaco de um adulto. Isso é detectado com anticorpos específicos projetados contra a extremidade N-terminal de sua sequência de aminoácidos.
Os testes de “nova geração” para a subunidade T da isoforma cardíaca prestam muita atenção ao fato de que alguns tecidos musculares esqueléticos lesionados podem reexprimir essa isoforma, para que possam ser obtidas reações cruzadas com os anticorpos.
Referências
- Babuin, L. & Jaffe, AS (2005). Troponina: o biomarcador de escolha para a detecção de lesão cardíaca. CMAJ , 173 (10), 1191-1202.
- Collinson, P., Stubbs, P., & Kessler, A.‑C. (2003). Avaliação multicêntrica do valor diagnóstico da troponina cardíaca T, massa de CK-MB e mioglobina na avaliação de pacientes com suspeita de síndromes coronárias agudas na prática clínica de rotina. Heart , 89 , 280-286.
- Farah, C. & Reinach, F. (1995). O complexo troponina e regulação da contração muscular. FASEB , 9 , 755-767.
- Keller, T., Peetz, D., Tzikas, S., Roth, A., Czyz, E., Bickel, C., … Blankenberg, S. (2009). Ensaio de troponina I sensível no diagnóstico precoce de infarto agudo do miocárdio. The New England Journal of Medicine , 361 (9), 868-877.
- Ross, M. & Pawlina, W. (2006). Histologia A Text and Atlas com correlação celular e biologia molecular (5ª ed.). Lippincott Williams e Wilkins.
- Wakabayashi, T. (2015). Mecanismo de regulação do cálcio da contração muscular. Em busca de sua base estrutural. Proc. Jpn Acad. Ser. B , 91 , 321-350.