A calorimetria é uma área da física que estuda a transferência de calor entre corpos e seus efeitos. Ela é fundamental para entender processos como aquecimento, resfriamento e mudanças de estado físico de substâncias. Além disso, a calorimetria tem diversas aplicações práticas, como no design de sistemas de refrigeração, na produção de energia e na indústria alimentícia, onde é utilizada para determinar o valor calórico dos alimentos. Neste contexto, o estudo da calorimetria é essencial para compreender e controlar os processos térmicos em diversos setores da ciência e da tecnologia.
Aplicações práticas da calorimetria: onde e como podemos utilizar essa importante técnica.
A calorimetria é uma técnica importante que estuda a transferência de calor entre corpos e seus efeitos. Ela possui diversas aplicações práticas em diferentes áreas, sendo fundamental para entender e controlar processos térmicos.
Uma das principais aplicações da calorimetria é na indústria alimentícia, onde é utilizada para determinar a quantidade de calorias presentes nos alimentos. Isso é essencial para a elaboração de dietas balanceadas e para garantir a qualidade dos produtos. Além disso, a calorimetria também é fundamental na conservação de alimentos, auxiliando no controle de temperaturas durante o armazenamento e transporte.
Na área da saúde, a calorimetria é utilizada em diversos procedimentos médicos, como na determinação do metabolismo basal de pacientes. Isso é importante para o tratamento de doenças relacionadas ao metabolismo e para a prescrição de dietas adequadas. Além disso, a calorimetria também é empregada em equipamentos médicos, como ressonâncias magnéticas, para garantir o correto funcionamento dos mesmos.
Outra aplicação importante da calorimetria é na indústria química, onde é utilizada para controlar reações químicas e processos de fabricação. Por meio da calorimetria, é possível determinar a quantidade de calor envolvida em uma reação, auxiliando na otimização de processos e na redução de custos. Além disso, a calorimetria também é essencial para garantir a segurança em processos que envolvem altas temperaturas.
Em resumo, a calorimetria é uma técnica fundamental com diversas aplicações práticas em diferentes áreas, contribuindo para o desenvolvimento de novos produtos, para a manutenção da saúde e para a segurança em processos industriais. Portanto, é essencial compreender e aplicar os conceitos da calorimetria para garantir eficiência e qualidade em diversas atividades do nosso cotidiano.
Entenda o conceito de calorimetria e sua área de estudo na física térmica.
A calorimetria é uma área da física térmica que estuda a quantidade de calor envolvida em processos físicos e químicos. Ela é responsável por medir as variações de temperatura e calcular a quantidade de calor trocada entre corpos em interação.
Na calorimetria, utilizamos instrumentos como os calorímetros para medir as trocas de calor. Esses aparelhos são compostos por materiais que possuem uma capacidade térmica conhecida, permitindo calcular a quantidade de calor envolvida em um determinado processo.
Além disso, a calorimetria estuda as propriedades térmicas dos materiais, como a condutividade térmica e o calor específico, que são essenciais para entender como os corpos reagem às variações de temperatura.
As aplicações da calorimetria são vastas e abrangem diversas áreas, desde a indústria até a medicina. Na indústria, por exemplo, ela é fundamental para o controle de processos de produção que envolvem reações químicas exotérmicas ou endotérmicas. Na medicina, a calorimetria é utilizada para diagnosticar e monitorar doenças que causam alterações na temperatura do corpo.
Em resumo, a calorimetria é uma ferramenta essencial para compreender as trocas de calor e as variações de temperatura nos mais diversos processos, contribuindo para o avanço da ciência e o desenvolvimento de novas tecnologias.
Locais de aplicação da calorimetria em diversas áreas da ciência e engenharia.
A calorimetria é uma área da física que estuda a transferência de calor entre sistemas e suas consequências. Ela possui diversas aplicações em diferentes campos da ciência e engenharia, sendo essencial para o desenvolvimento de novas tecnologias e processos.
Um dos principais locais de aplicação da calorimetria é na indústria, onde é utilizada para medir a quantidade de calor envolvida em reações químicas e processos de fabricação. Isso permite otimizar a eficiência energética e garantir a qualidade dos produtos. Além disso, a calorimetria é fundamental para o desenvolvimento de novos materiais com propriedades térmicas específicas.
Na área da medicina, a calorimetria é empregada para estudar o metabolismo humano e diagnosticar doenças relacionadas com o desequilíbrio térmico do corpo. Ela também é utilizada em pesquisas sobre tratamentos térmicos e no desenvolvimento de equipamentos médicos.
Em pesquisas acadêmicas, a calorimetria é aplicada para investigar fenômenos térmicos em diversos sistemas, como materiais, fluidos e compostos químicos. Ela é essencial para entender as propriedades térmicas dos materiais e contribui para o avanço do conhecimento científico.
Na engenharia, a calorimetria é utilizada para projetar sistemas de refrigeração, aquecimento e isolamento térmico, garantindo o funcionamento adequado de máquinas e equipamentos. Ela também é empregada no desenvolvimento de novas tecnologias sustentáveis, visando a redução do consumo de energia e a minimização do impacto ambiental.
Em resumo, a calorimetria é uma ferramenta fundamental em diversas áreas da ciência e engenharia, contribuindo para a compreensão dos processos térmicos e para o desenvolvimento de novas tecnologias e aplicações. Seu estudo e aplicação são essenciais para o avanço da sociedade e para a busca de soluções inovadoras para os desafios do mundo moderno.
Princípios básicos da calorimetria: descubra como medir e calcular a energia térmica.
A calorimetria é uma área da física que estuda as trocas de energia térmica entre corpos. Para medir e calcular essa energia, é importante conhecer alguns princípios básicos da calorimetria.
Um dos princípios fundamentais é a Lei da Conservação da Energia, que afirma que a energia total de um sistema isolado permanece constante ao longo do tempo. Isso significa que a energia térmica perdida por um corpo será igual à energia térmica ganha por outro corpo em um processo de troca de calor.
Outro princípio importante é a capacidade térmica, que representa a quantidade de calor necessária para elevar a temperatura de um corpo em uma unidade de temperatura. A capacidade térmica é uma propriedade específica de cada material e pode ser utilizada para calcular a quantidade de calor envolvida em um processo térmico.
Para medir a energia térmica envolvida em um processo, utilizamos um instrumento chamado calorímetro. O calorímetro é um dispositivo que permite isolar o sistema do ambiente externo e medir com precisão as trocas de calor entre corpos.
Para calcular a energia térmica, utilizamos a fórmula Q = mcΔT, onde Q representa a quantidade de calor, m a massa do corpo, c a capacidade térmica e ΔT a variação de temperatura. Com essa fórmula, podemos determinar a quantidade de energia térmica envolvida em um processo e realizar diversos cálculos relacionados à calorimetria.
A calorimetria tem diversas aplicações práticas, como no estudo de processos industriais, na determinação de capacidades térmicas de materiais e no cálculo de trocas de calor em sistemas complexos. Com o conhecimento dos princípios básicos da calorimetria, é possível compreender e analisar de forma precisa as trocas de energia térmica em diversos contextos.
Calorimetria: o que você estuda e aplicações
A calorimetria é uma técnica que determina as mudanças do conteúdo calórico de um sistema relacionado com um processo químico ou físico. É baseado na medição de mudanças de temperatura quando um sistema absorve ou emite calor. O calorímetro é o equipamento usado nas reações nas quais uma troca de calor está envolvida.
O que é conhecido como “xícara de café” é a forma mais simples desse tipo de dispositivo. Ao usá-lo, a quantidade de calor envolvida nas reações realizadas a pressão constante em uma solução aquosa é medida. Um calorímetro de xícara de café consiste em um recipiente de poliestireno, que é colocado em um copo.

A água é colocada no recipiente de poliestireno, equipado com uma tampa do mesmo material que proporciona um certo grau de isolamento térmico. Além disso, a embalagem possui um termômetro e um agitador mecânico.
Nesse calorímetro, mede-se a quantidade de calor que é absorvido ou emitido, dependendo se a reação é endotérmica ou exotérmica, quando uma reação ocorre em uma solução aquosa. O sistema a ser estudado consiste em reagentes e produtos.
O que estuda a calorimetria?
A calorimetria estuda a relação da energia térmica associada a uma reação química e como é usada para determinar suas variáveis. Suas aplicações nos campos de pesquisa justificam o escopo desses métodos.
Capacidade calórica de um calorímetro
Essa capacidade é calculada dividindo a quantidade de calor absorvido pelo calorímetro, variando a temperatura. Essa variação é um produto do calor emitido em uma reação exotérmica, que é igual a:
Quantidade de calor absorvido pelo calorímetro + quantidade de calor absorvido pela solução
A variação pode ser determinada adicionando uma quantidade conhecida de calor medindo a mudança de temperatura. Para esta determinação da capacidade calórica, o ácido benzóico é normalmente usado, uma vez que seu calor de combustão é conhecido (3.227 kJ / mol).
A capacidade calórica também pode ser determinada pela adição de calor por uma corrente elétrica.
Exemplo de uso do calorímetro para calcular o calor específico
Uma barra de 95 g de um metal é aquecida a 400 ° C, sendo imediatamente levada para um calorímetro com 500 g de água, inicialmente a 20 ° C. A temperatura final do sistema é de 24 ° C. Calcule o calor específico do metal.
Δq = mx ce x Δt
Nesta expressão:
Δq = variação de carga.
m = massa
ce = calor específico.
Δt = variação de temperatura.
O calor ganho pela água é igual ao calor liberado pela barra de metal.
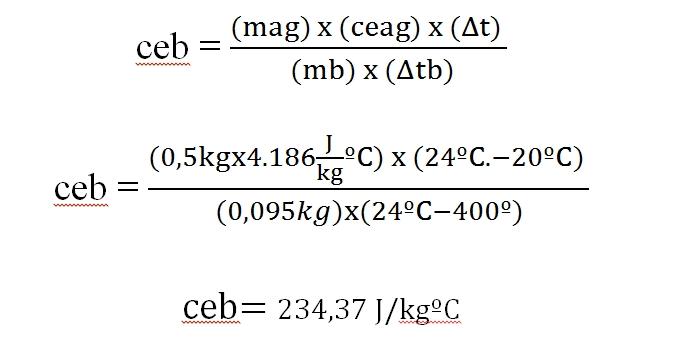
Esse valor é semelhante ao mostrado em uma tabela de calor específica para prata (234 J / kg ° C).
Então, uma das aplicações da calorimetria é a cooperação para a identificação de materiais.
Bomba calorimétrica
Consiste em um recipiente de aço, conhecido como bomba, resistente às altas pressões que podem surgir durante as reações que ocorrem nesse recipiente; Este recipiente está conectado a um circuito de ignição para iniciar as reações.
A bomba é imersa em um grande recipiente com água, cuja função é absorver o calor que é gerado na bomba durante as reações, diminuindo a variação de temperatura. O reservatório de água está equipado com um termômetro e um agitador mecânico.
As mudanças de energia são medidas praticamente em volume e temperatura constantes, de modo que nenhum trabalho é realizado sobre as reações que ocorrem na bomba.
ΔE = q
ΔE é a variação da energia interna na reação e q o calor gerado nela.
Tipos de calorímetro
Calorímetro de titulação isotérmica (CTI)
O calorímetro possui duas células: em uma a amostra é colocada e na outra, a referência, a água é geralmente colocada.
A diferença de temperatura que é gerada entre as células – devido à reação que ocorre na célula de amostra – é anulada por um sistema de feedback que injeta calor para igualar as temperaturas das células.
Este tipo de calorímetro permite acompanhar a interação entre macromoléculas e seus ligantes.
Calorímetro diferencial de varredura
Esse calorímetro possui duas células, assim como o CTI, mas possui um dispositivo que permite determinar os fluxos de temperatura e calor associados às mudanças de um material em função do tempo.
Esta técnica fornece informações sobre o dobramento de proteínas e ácidos nucléicos, bem como sua estabilização.
Aplicações

-A calorimetria permite determinar a troca de calor que ocorre em uma reação química, permitindo entender mais claramente o mecanismo disso.
– Ao determinar o calor específico de um material, a calorimetria fornece dados que ajudam na sua identificação.
-Como existe uma proporcionalidade direta entre a mudança de calor de uma reação e a concentração dos reagentes, juntamente com o fato de a calorimetria não exigir amostras claras, essa técnica pode ser usada para determinar a concentração de substâncias presentes em matrizes complexas.
-No campo da engenharia química, a calorimetria é usada no processo de segurança, bem como em diferentes campos do processo de otimização, reação química e na unidade operacional.
Usos de calorimetria de titulação isotérmica
-Colabora no estabelecimento do mecanismo de ação enzimática, bem como em sua cinética. Essa técnica pode medir reações entre moléculas, determinando afinidade de ligação, estequiometria, entalpia e entropia em solução sem a necessidade de marcadores.
-Avalia a interação de nanopartículas com proteínas e, em conjunto com outros métodos analíticos, é uma ferramenta importante para o registro de alterações conformacionais nas proteínas.
-Tem aplicação em preservação de alimentos e lavouras.
-Quanto à preservação de alimentos, pode determinar sua deterioração e prazo de validade (atividade microbiológica). Ele pode comparar a eficiência de diferentes métodos de preservação de alimentos e é capaz de determinar a dose ideal de conservantes, bem como a degradação no controle de embalagens.
-Quanto às culturas vegetais, você pode estudar a germinação das sementes. Estando na água e na presença de oxigênio, eles liberam calor que pode ser medido com um calorímetro isotérmico. Examine a idade e o armazenamento inadequado das sementes e estude sua velocidade de crescimento diante de variações de temperatura, pH ou de diferentes produtos químicos.
-Finalmente, você pode medir a atividade biológica dos solos. Além disso, ele pode detectar doenças.
Usos da calorimetria diferencial de varredura
– Juntamente com a calorimetria isotérmica, permitiu estudar a interação de proteínas com seus ligantes, a interação alostérica, o dobramento das proteínas e o mecanismo de sua estabilização.
-Você pode medir diretamente o calor liberado ou absorvido durante um evento de ligação molecular.
A calorimetria diferencial de varredura é uma ferramenta termodinâmica para o estabelecimento direto da coleta de energia calórica que ocorre em uma amostra. Isso permite analisar os fatores envolvidos na estabilidade da molécula de proteína.
-Estuda também a termodinâmica da transição da dobragem de ácidos nucleicos. A técnica permite a determinação da estabilidade oxidativa do ácido linoléico isolado e acoplado a outros lipídios.
-A técnica é aplicada na quantificação de nanossólidos farmacêuticos para uso e na caracterização térmica de transportadores lipídicos nanoestruturados.
Referências
- Whitten, K., Davis, R., Peck, M. e Stanley, G. Chemistry . (2008). 8th ed. Cengage Learning Edit.
- Rehak, NN e Young, DS (1978). Aplicações prospectivas de calorimetria no laboratório clínico. Clin. Chem. 24 (8): 1414-1419.
- Stossel, F. (1997). Aplicações da calorimetria de reação em engenharia química . J. Therm. Anal. 49 (3): 1677-1688.
- Weber, PC e Salemme, FR (2003). Aplicações de métodos calorimétricos à descoberta de drogas e ao estudo de interações proteicas . Curr. Opin. Struct. Biol.13 (1): 115-121.
- Gill, P., Moghadem, T. e Ranjbar, B. (2010).Técnicas calorimétricas de varredura diferencial: aplicações em biologia e nanociência . J. Biol. Tech. 21 (4): 167-193.
- Omanovic-Miklicanin, E., Manfield, I. e Wilkins, T. (2017). Aplicações da calorimetria de titulação isotérmica na avaliação de interações proteína-nanopartículas . J. Therm. Anal. 127: 605-613.
- Consórcio do Community College para credenciais de biociência. (7 de julho de 2014). Calorímetro de xícara de café. [Figura]. Recuperado em 7 de junho de 2018, de: commons.wikimedia.org