O hidróxido de cobre (II) é um composto químico formado pela ligação do íon cobre (II) com o íon hidróxido. Sua fórmula química é Cu(OH)2 e sua estrutura cristalina é constituída por íons de cobre (II) rodeados por íons hidróxido. Possui uma coloração azul clara e é pouco solúvel em água.
Em relação às suas propriedades, o hidróxido de cobre (II) é um material estável à temperatura ambiente, porém pode se decompor em altas temperaturas, liberando oxigênio e formando óxido de cobre (II). Além disso, é um composto tóxico e corrosivo, devendo ser manuseado com cuidado.
Quanto à nomenclatura, o hidróxido de cobre (II) segue as regras da IUPAC, sendo chamado de hidróxido de cobre (II) para indicar o metal e o grau de oxidação do íon cobre.
Em termos de usos, o hidróxido de cobre (II) é utilizado como fungicida na agricultura, para proteger plantas de doenças fúngicas. Também é empregado na indústria de pigmentos, na produção de tintas e corantes, e como catalisador em reações químicas. Sua aplicação mais comum é na fabricação de baterias recarregáveis de íon-lítio, devido à sua capacidade de armazenar e liberar energia de forma eficiente.
Benefícios e aplicações do óxido de cobre na indústria e na saúde.
O óxido de cobre é um composto químico com diversas aplicações na indústria e na saúde. Na indústria, ele é amplamente utilizado como catalisador em reações químicas, na produção de tintas e pigmentos, na fabricação de cerâmicas e na indústria de semicondutores. Além disso, o óxido de cobre é um componente essencial em baterias recarregáveis e em dispositivos eletrônicos.
Na saúde, o óxido de cobre é utilizado em diversas aplicações, como na fabricação de suplementos alimentares de cobre, na produção de medicamentos antifúngicos e como agente bactericida em produtos de limpeza e desinfetantes. Além disso, o óxido de cobre é utilizado em tratamentos dermatológicos para promover a cicatrização de feridas e na prevenção de infecções cutâneas.
Os benefícios do óxido de cobre na indústria e na saúde são inegáveis, tornando-o um composto químico de grande importância em diversos setores. Sua versatilidade e eficácia o tornam indispensável em muitos processos e produtos.
Significado e propriedades do hidróxido de bário, também conhecido como BA Oh 2.
O hidróxido de bário, também conhecido como Ba(OH)2, é um composto químico formado por um átomo de bário e dois átomos de hidrogênio ligados a um átomo de oxigênio. Este composto é classificado como uma base forte devido à sua capacidade de ionizar-se completamente em solução aquosa, liberando íons de hidróxido (OH-) que aumentam o pH da solução.
O hidróxido de bário é uma substância sólida, branca e cristalina, altamente solúvel em água. É um composto tóxico e corrosivo, devendo ser manuseado com cuidado e seguindo as devidas precauções de segurança. Além disso, é utilizado em diversas aplicações industriais, como na fabricação de vidros, pigmentos e produtos químicos.
Uma das propriedades mais importantes do hidróxido de bário é sua capacidade de reagir com ácidos, formando sais e água. Essa reação é conhecida como neutralização e é amplamente utilizada em processos químicos e na indústria.
Em relação ao hidróxido de cobre (II), este composto é formado pela ligação de um átomo de cobre com dois átomos de hidrogênio e um átomo de oxigênio. Assim como o hidróxido de bário, o hidróxido de cobre (II) é uma base forte e possui propriedades similares, incluindo a capacidade de aumentar o pH de uma solução aquosa.
Em termos de nomenclatura, o hidróxido de cobre (II) é conhecido como Cu(OH)2, indicando a presença do íon de cobre com valência +2 e do íon de hidróxido. Este composto é utilizado em diversas aplicações, como na fabricação de tintas, fertilizantes e produtos químicos.
Ambos devem ser manuseados com cuidado devido à sua toxicidade e corrosividade, mas são essenciais para diversos processos químicos e produtos do nosso dia a dia.
Dicas práticas para utilizar o óxido de cobre de forma eficiente e sustentável.
O óxido de cobre é um composto químico amplamente utilizado em diversas aplicações industriais e domésticas. Para garantir sua eficiência e sustentabilidade, é importante seguir algumas dicas práticas. Uma delas é armazenar o óxido de cobre em local seco e bem ventilado, longe de fontes de calor e umidade, para evitar sua deterioração. Além disso, é recomendável utilizar equipamentos de proteção individual ao manusear o composto, como luvas e óculos de segurança.
Outra dica importante é utilizar o óxido de cobre em quantidades adequadas, seguindo as recomendações de uso do fabricante. O excesso de composto pode ser prejudicial ao meio ambiente e à saúde humana. Além disso, é fundamental descartar corretamente o óxido de cobre, seguindo as normas de reciclagem e descarte de resíduos químicos.
Por fim, para garantir a eficiência do óxido de cobre, é importante armazená-lo em embalagens adequadas e identificadas, evitando assim sua contaminação e deterioração. Seguindo essas dicas práticas, é possível utilizar o óxido de cobre de forma eficiente e sustentável em diversas aplicações.
Identifique o nome da base CsOH utilizada em química.
O Hidróxido de cobre (II) é uma base química que possui diversas aplicações e propriedades interessantes. É importante ressaltar que a base CsOH é o hidróxido de césio, não o hidróxido de cobre (II).
O hidróxido de cobre (II) é composto por íons de cobre (Cu2+) e íons hidróxido (OH-) e apresenta uma estrutura cristalina. Sua fórmula química é Cu(OH)2 e é conhecido por suas propriedades como um sólido azul ou verde, dependendo da forma como é preparado.
Em relação às propriedades, o hidróxido de cobre (II) é pouco solúvel em água e possui propriedades básicas, podendo reagir com ácidos para formar sais de cobre. Além disso, é um material utilizado em diversos processos industriais e em laboratórios de química.
Quanto à nomenclatura, o hidróxido de cobre (II) recebe esse nome devido à presença do íon de cobre com carga +2, indicando que o cobre está em seu estado de oxidação +2.
Em relação aos usos, o hidróxido de cobre (II) é utilizado na produção de pigmentos, na fabricação de baterias recarregáveis e como catalisador em reações químicas. Sua versatilidade e propriedades o tornam um composto importante na indústria química.
Hidróxido de cobre (II): estrutura, propriedades, nomenclatura, usos
O hidróxido de cobre (II) ou de hidróxido cúprico é azul ou azul pálido – cristalino verde sólido inorgânico com a fórmula química Cu (OH) 2 . É obtido como um precipitado azul volumoso adicionando um hidróxido alcalino a soluções cupic (significa que elas contêm íons Cu 2+ ). É um pouco composto estável.
Para aumentar a estabilidade é preparado na presença de amónia (NH 3 ) ou fosfatos.Si preparado na presença de amónia num material com uma boa estabilidade e tamanho de partícula grande ocorre.
Quando é preparada a partir de fosfato de cobre (II), Cu 3 (PO 4 ) 2 , um material é obtido com tamanho de partícula mais fina e uma área de superfície maior.O hidróxido cúprico é amplamente utilizado como fungicida e bactericida na agricultura e no tratamento de madeira, prolongando sua vida útil.
Também é usado como um complemento nutricional para animais. É usado como matéria-prima para obter outros sais de cobre (II) e na galvanoplastia para revestir superfícies.
Estão sendo realizados estudos para estimar seu potencial para combater infecções bacterianas e fúngicas em humanos.
Estrutura
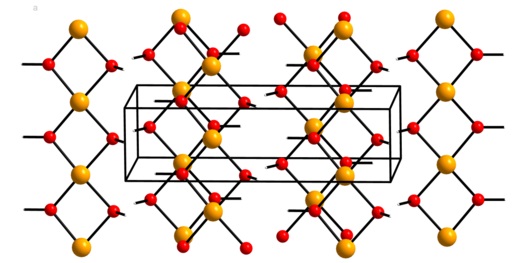
O hidróxido de cobre (II) contém cadeias infinitas de íons de cobre (Cu 2+ ) unidos por pontes do grupo hidroxila (OH – ).
As cadeias são tão compactadas que 2 átomos de oxigênio de outras cadeias estão acima e abaixo de cada átomo de cobre, adotando uma configuração octaédrica distorcida, que é comum na maioria dos compostos de cobre (II).
Em sua estrutura, quatro átomos de oxigênio estão a uma distância de 1,93 A; dois átomos de oxigênio estão em 2,63 A; e a distância Cu-Cu é 2,95 A.
Nomenclatura
– Hidróxido de cobre (II).
– Hidróxido cúprico.
– Dihidróxido de cobre.
Propriedades
Estado físico
Sólido cristalino.
Peso molecular
99,58 g / mol.
Ponto de fusão
Decompõe-se antes de derreter. Ponto de degradação 229 ° C.
Densidade
3,37 g / cm 3
Solubilidade
É praticamente insolúvel em água: 2,9 microgramas / L a 25 ° C. Rapidamente solúvel em ácidos, em soluções alcalinas concentradas e em hidróxido de amônio. Insolúvel em solventes orgânicos. Na água quente, decompõe-se gerando óxido de cobre (II), que é mais estável.
Outras propriedades
É facilmente solúvel em ácidos fortes e também em soluções alcalinas concentradas de hidróxidos, para fornecer ânions azuis profundos, provavelmente do tipo [Cu n (OH) 2n + 2 ] 2- .
Sua estabilidade depende do método de preparação.
Ele pode ser decomposto fornecendo óxido de cobre preto (II) (CuO) se permanecer em repouso por alguns dias ou sob aquecimento.
Na presença de um excesso de álcalis, decompõe-se acima de 50 ° C.
Usos
Na agricultura
O hidróxido de cobre (II) tem uma ampla aplicação como fungicida e antibacteriano em culturas agrícolas. Aqui estão alguns exemplos:
– Serve contra manchas bacterianas ( Erwinia ) na alface, aplicadas como tratamento foliar.
– Contra manchas bacterianas (de Xanthomonas pruni ) em pêssegos, para os quais é aplicado um tratamento latente e foliar.
– É usado contra a praga de folhas e caule de mirtilos por aplicações latentes.
– Contra a podridão durante o armazenamento de mirtilos causados por Monilinia oxycocci , por aplicação latente.
Para aplicação na agricultura, é usado hidróxido de cobre (II), que é preparado na presença de fosfatos devido ao seu pequeno tamanho de partícula.
Na preservação de madeira
A madeira, sendo de natureza orgânica, é sensível ao ataque de insetos e microorganismos. O hidróxido de cobre (II) é usado como biocida para fungos que atacam a madeira.
É geralmente usado em conjunto com um composto de amônio quaternário (NH 4 + ). O hidróxido de cobre atua como fungicida e o composto de amônio quaternário funciona como inseticida.
Dessa maneira, a madeira tratada suporta ou resiste às condições de serviço, atingindo o nível de desempenho exigido pelo usuário.No entanto, a madeira tratada com esses compostos tem um alto nível de cobre e é muito corrosiva para o aço comum; portanto, é necessário um tipo de aço inoxidável que possa suportar o processamento da madeira tratada.
Apesar de sua utilidade, o hidróxido de cobre (II) é considerado um biocida levemente perigoso.
Por esse motivo, existe a preocupação de que ela seja liberada da madeira tratada para o meio ambiente em quantidades que possam ser prejudiciais aos microorganismos naturalmente presentes na água (rios, lagos, pântanos e mar) ou no solo.
Na fabricação de rayon
Desde o século 19, soluções amoniacais de hidróxido de cobre (II) têm sido usadas para dissolver a celulose. Este é um dos primeiros passos para obter a fibra chamada rayon através da tecnologia desenvolvida por Bemberg na Alemanha.
O hidróxido de cobre (II) se dissolve em uma solução de amônia (NH 3 ), formando um sal complexo.
As fibras de algodão curtas refinadas são adicionadas à solução de amônia de cobre contendo o hidróxido de cobre (II) como um sólido precipitado.
A celulose de algodão forma um complexo com hidróxido de cobre tetra-amônio dissolvido na solução.
Posteriormente, esta solução coagula enquanto se apresenta como um dispositivo de extrusão.
Devido ao seu alto custo, essa tecnologia já foi superada pela viscose. Atualmente, a tecnologia de Bemberg é usada apenas no Japão.
Na indústria de ração animal
É usado como vestígios na alimentação animal, pois é uma das substâncias necessárias como micronutrientes para a nutrição completa dos animais.
Isso ocorre porque nos seres vivos superiores, o cobre é um elemento essencial, necessário para a atividade de uma variedade de enzimas que contêm cobre.
Por exemplo, está contido na enzima que participa da produção de colágeno e na enzima necessária para a síntese de melanina, entre outros.
É um composto geralmente reconhecido como seguro quando adicionado a níveis consistentes com as boas práticas de alimentação.
Na fabricação de outros compostos de cobre (II)
Precursor ativo na produção dos seguintes compostos de cobre (II): naftenato de cobre (II), 2-etil-hexanoato de cobre (II) e sabões de cobre.Nesses casos, é usado hidróxido de cobre (II), que é sintetizado na presença de amônia.
Outros usos
É utilizado na estabilização do nylon, em eletrodos de bateria; como fixador de cor em operações de tingimento; como pigmento; em inseticidas; no tratamento e coloração de papel; em catalisadores, como catalisador na vulcanização da borracha de polissulfeto; como pigmento antiincrustante; e em eletrólise, em galvanoplastia.
Futuras aplicações médicas
O hidróxido de cobre (II) faz parte dos compostos de cobre que estão sendo estudados na forma de nanopartículas para a eliminação de bactérias como E. coli , K. pneumoniae, P. aeruginosa, Salmonella spp. , entre outros, causando doenças em seres humanos.
Também foi descoberto que as nanopartículas de cobre podem ser eficazes contra Candida albicans , um fungo que é uma causa comum de patologias humanas.
Isso indica que a nanotecnologia do cobre pode desempenhar um papel importante contra bactérias e fungos que causam infecções humanas, e o hidróxido de cobre (II) pode ser muito útil nesses campos.
Referências
- Cotton, F. Albert e Wilkinson, Geoffrey. (1980). Química Inorgânica Avançada. Quarta Edição John Wiley & Sons.
- Kirk-Othmer (1994). Enciclopédia de Tecnologia Química. Volume 7. Quarta Edição. John Wiley & Sons.
- Enciclopédia de Química Industrial de Ullmann. (1990). Quinta Edição Volume A7. VCH Verlagsgesellschaft mbH.
- Dançando, JC; Emeléus, HJ; Sir Ronald Nyholm e Trotman-Dickenson, AF (1973). Química Inorgânica Abrangente. Volume 3. Pergamon Press.
- Biblioteca Nacional de Medicina (2019). Hidróxido de cobre (II). Recuperado de: pubchem.ncbi.nlm.nih.gov
- Schiopu, N. e Tiruta-Barna, L. (2012). Conservantes de madeira Em Toxicidade de materiais de construção. Capítulo 6. Recuperado de sciencedirect.com.
- Mordorski, B. e Friedman, A. (2017). Nanopartículas de metal para infecção microbiana. Em nanomateriais funcionalizados para o manejo da infecção microbiana. Capítulo 4. Recuperado de sciencedirect.com.
- Takashi Tsurumi (1994). Solução girando Em tecnologia avançada de fiação de fibra. Capítulo 3. Recuperado de sciencedirect.com.