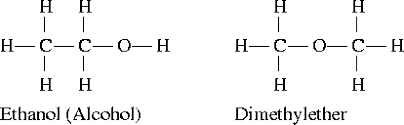
Isomerismo é um fenômeno químico no qual compostos diferentes possuem a mesma fórmula molecular, mas estruturas moleculares diferentes. Existem diversos tipos de isômeros, como isômeros constitucionais, estereoisômeros e tautômeros, que apresentam características distintas em relação à disposição dos átomos na molécula. Neste artigo, abordaremos os principais tipos de isômeros e forneceremos exemplos para ilustrar cada um deles.
Isômeros: definição e exemplos de compostos com mesma fórmula molecular, mas estruturas diferentes.
Os isômeros são compostos que possuem a mesma fórmula molecular, mas estruturas diferentes. Isso significa que eles têm os mesmos átomos, mas estão arranjados de maneira distinta, resultando em propriedades químicas e físicas diferentes.
Existem diferentes tipos de isomerismo, como isomeria plana, espacial e de função. Na isomeria plana, os átomos estão dispostos de forma diferente no plano, enquanto na isomeria espacial, a disposição dos átomos ocorre no espaço tridimensional. Já na isomeria de função, os compostos possuem grupos funcionais diferentes, mas a mesma fórmula molecular.
Um exemplo clássico de isomerismo são os isômeros C4H10, que podem ser representados pelo n-butano e isobutano. Ambos possuem a mesma fórmula molecular, mas o n-butano possui uma cadeia linear de quatro átomos de carbono, enquanto o isobutano possui uma ramificação em sua estrutura.
Outro exemplo são os isômeros C6H12O6, que são a glicose e frutose. Ambos são monossacarídeos com a mesma fórmula molecular, porém suas estruturas são diferentes, o que resulta em propriedades distintas, como sabor e solubilidade.
Em resumo, os isômeros são compostos com a mesma fórmula molecular, mas estruturas diferentes, o que os torna distintos em termos de propriedades químicas e físicas. O estudo do isomerismo é fundamental na química orgânica para compreender a diversidade e complexidade dos compostos químicos.
Tipos de isômeros: conheça as diferentes formas de arranjo molecular dos compostos.
O isomerismo é um fenômeno muito comum na química, onde compostos com a mesma fórmula molecular podem ter arranjos diferentes de seus átomos. Existem diversos tipos de isômeros, que podem ser classificados de acordo com suas características estruturais. Vamos conhecer alguns deles.
Um dos tipos mais comuns de isômeros são os isômeros constitucionais, também conhecidos como isômeros estruturais. Esses isômeros possuem a mesma fórmula molecular, mas seus átomos estão arranjados de maneira diferente. Um exemplo clássico desse tipo de isomerismo é o caso do metanol e do éter dimetílico.
Outro tipo de isômero são os isômeros geométricos, que ocorrem em compostos que apresentam ligação dupla ou anel ciclano. Nesse caso, os átomos estão dispostos de forma diferente no espaço, o que resulta em propriedades físicas e químicas distintas. Um exemplo comum de isômeros geométricos são os isômeros cis e trans de compostos orgânicos.
Além disso, existem os isômeros ópticos, que se diferenciam pela forma como interagem com a luz polarizada. Esses isômeros apresentam formas espaciais diferentes, conhecidas como enantiômeros, que são imagens espelhadas não superponíveis. Um exemplo de isômeros ópticos são os aminoácidos L e D.
Como podemos ver, os isômeros são uma parte importante da química orgânica, pois nos mostram como os mesmos átomos podem se organizar de diferentes maneiras, resultando em compostos com propriedades distintas. É fascinante observar essas diferentes formas de arranjo molecular e como elas influenciam as características dos compostos.
O que são isômeros e como eles se diferem?
Os isômeros são compostos que possuem a mesma fórmula molecular, mas estruturas químicas diferentes. Eles se diferem na disposição dos átomos, o que resulta em propriedades físicas e químicas distintas. O isomerismo é uma importante área da química que estuda essas variações nas estruturas moleculares.
Existem diversos tipos de isômeros, como os isômeros estruturais, que possuem diferentes arranjos de átomos, os isômeros de posição, que diferem na posição de um grupo funcional, os isômeros de função, que possuem grupos funcionais diferentes, e os isômeros geométricos, que diferem na orientação dos átomos em torno de uma ligação dupla ou tripla.
Um exemplo clássico de isomerismo são os isômeros de cadeia, como o n-butano e o isobutano. Ambos possuem a mesma fórmula molecular C4H10, mas apresentam cadeias carbônicas diferentes. Enquanto o n-butano possui uma cadeia linear, o isobutano possui uma ramificação em sua estrutura.
Em resumo, os isômeros são compostos que compartilham a mesma fórmula molecular, mas possuem estruturas químicas distintas. Essas diferenças na disposição dos átomos resultam em propriedades únicas para cada isômero, tornando o estudo do isomerismo uma área fundamental da química orgânica.
Isomeria de cadeia: conceito e exemplo prático.
Isomeria de cadeia é um tipo de isomeria em que os isômeros possuem a mesma fórmula molecular, mas diferem na disposição dos átomos na cadeia carbonada. Isso significa que as moléculas têm o mesmo número e tipo de átomos, mas estão dispostos de maneira diferente.
Um exemplo prático de isomeria de cadeia é o caso do butano e do metilpropano. Ambos têm a fórmula molecular C4H10, mas a forma como os átomos de carbono estão ligados na cadeia é diferente. No butano, temos uma cadeia linear de quatro átomos de carbono, enquanto no metilpropano temos uma cadeia ramificada, com um grupo metila ligado a um dos átomos de carbono.
Essa diferença na disposição dos átomos na cadeia faz com que esses isômeros de cadeia tenham propriedades físicas e químicas diferentes. Por exemplo, o butano é um gás à temperatura ambiente, enquanto o metilpropano é um líquido. Além disso, eles podem ter comportamentos químicos distintos devido à sua estrutura molecular única.
Portanto, a isomeria de cadeia é um fenômeno importante na química orgânica, pois nos permite entender como pequenas variações na estrutura molecular podem levar a diferenças significativas nas propriedades e no comportamento das substâncias.
Isomerismo: Tipos e Exemplos de Isômeros
O isomerismo relaciona-se com a existência de duas ou mais substâncias que têm a mesma fórmula molecular, mas cuja estrutura é diferente em cada um dos compostos. Nestas substâncias, conhecidas como isômeros, todos os elementos são apresentados na mesma proporção, mas formando uma estrutura de átomos que é diferente em cada molécula.
A palavra isômero vem da palavra grega isomerès , que significa “partes iguais”. Ao contrário do que se pode supor, e embora contenham os mesmos átomos, os isômeros podem ou não ter características semelhantes, dependendo dos grupos funcionais presentes em sua estrutura.
São conhecidas duas classes principais de isomerismo: isomerismo constitucional (ou estrutural) e estereoisomerismo (ou isomerismo espacial). O isomerismo ocorre tanto em substâncias orgânicas (álcoois, cetonas, entre outras) quanto em substâncias inorgânicas (compostos de coordenação).
Às vezes ocorrem espontaneamente; Nestes casos, os isômeros de uma molécula são estáveis e presentes em condições padrão (25 ° C, 1 atm), que constituíram um avanço muito importante no campo da química no momento de sua descoberta.
Tipos de isômeros
Como afirmado anteriormente, são apresentados dois tipos de isômeros que diferem pelo arranjo de seus átomos. Os tipos de isômeros são os seguintes:
Isômeros constitucionais (estruturais)
São os compostos que possuem os mesmos átomos e grupos funcionais, mas dispostos em uma ordem diferente; isto é, as ligações que compõem suas estruturas têm um arranjo diferente em cada composto.
Eles são divididos em três tipos: isômeros de posição, isômeros de cadeia ou esqueleto e isômeros de grupos funcionais, às vezes chamados de isômeros funcionais.
Isômeros de posição
Eles têm os mesmos grupos funcionais, mas estes são encontrados em um local diferente em cada molécula.
Isômeros de cadeia ou esqueleto
Eles se distinguem pela distribuição de substituintes de carbono no composto, isto é, pela maneira como são distribuídos linearmente ou ramificados.
Isômeros de grupo funcional
Também chamados de isômeros funcionais, eles consistem nos mesmos átomos, mas formam grupos funcionais diferentes em cada molécula.
Tautomería
Existe uma classe excepcional de isomerismo chamada tautomia, na qual há uma interconversão de uma substância em outra que geralmente é dada pela transferência de um átomo entre os isômeros, causando um equilíbrio entre essas espécies.
Estereoisômeros (isômeros espaciais)
Esse é o nome de substâncias que possuem exatamente a mesma fórmula molecular e cujos átomos são organizados na mesma ordem, mas cuja orientação no espaço difere entre eles. Portanto, para garantir sua visualização correta, eles devem ser representados de maneira tridimensional.
Em termos gerais, existem dois tipos de estereoisômeros: isômeros geométricos e isômeros ópticos.
Isômeros geométricos
Eles são formados pela quebra de uma ligação química no composto. Essas moléculas são apresentadas em pares que diferem em suas propriedades químicas, para diferenciá-las foram estabelecidos os termos cis (substituintes específicos em posições adjacentes) e trans (substituintes específicos em posições opostas de sua fórmula estrutural).
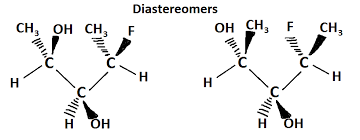
Nesse caso, destacam-se os diastereômeros, que têm configurações diferentes e não são sobrepostos entre si, cada um com suas próprias características. Existem também isômeros conformacionais, formados pela rotação de um substituinte em torno de uma ligação química.
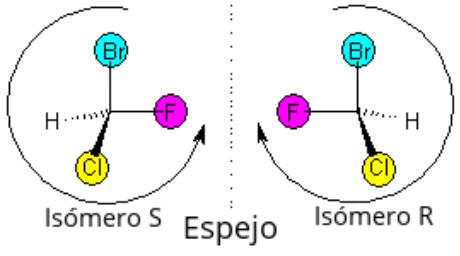
Isômeros ópticos
Eles são aqueles que constituem imagens de espelho que não podem ser sobrepostas; isto é, se a imagem de um isômero é colocada na imagem do outro, a posição de seus átomos não corresponde exatamente. No entanto, eles têm as mesmas características, mas diferem na interação com a luz polarizada.
Nesse grupo, destacam-se os enantiômeros, que geram a polarização da luz de acordo com seu arranjo molecular e se distinguem como dextrogíricos (se a polarização da luz estiver na direção correta do plano) ou levógiro (se a polarização estiver na direção esquerda) do avião).
Quando existe a mesma quantidade de ambos os enantiômeros (dyl), a polarização líquida ou resultante é zero, o que é conhecido como mistura racêmica.
Exemplos de isômeros
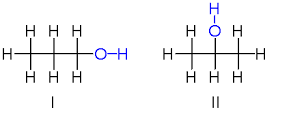
Primeiro exemplo
O primeiro exemplo apresentado é o dos isômeros de posição estrutural, nos quais existem duas estruturas com a mesma fórmula molecular (C 3 H 8 O), mas cujo substituinte -OH está em duas posições diferentes, formando 1-propanol (I) e 2-propanol (II).
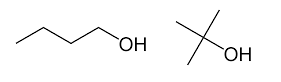
Segundo exemplo
Neste segundo exemplo, dois isômeros estruturais de cadeia ou esqueleto são observados; ambos têm a mesma fórmula (C 4 H 10 O) e o mesmo substituinte (OH), mas o isômero à esquerda é de cadeia linear (1-butanol), enquanto o da direita tem uma estrutura ramificada (2-metil-2 -propanol).
Terceiro exemplo
Dois isômeros estruturais do grupo funcional também são mostrados abaixo, onde ambas as moléculas possuem exatamente os mesmos átomos (com fórmula molecular C 2 H 6 O), mas seu arranjo é diferente, resultando em álcool e éter, cujas propriedades físicas e químicas Eles variam muito de um grupo funcional para outro.
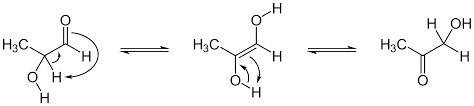
Quarto exemplo
Além disso, um exemplo de tautomería é o equilíbrio entre algumas estruturas com grupos funcionais C = O (cetonas) e OH (álcoois), também chamados de equilíbrio ceto-enólico.
Quinto exemplo
A seguir, são apresentados dois isômeros cis e trans-geométricos, observando que o da esquerda é o isômero cis, que é indicado com a letra Z em sua nomenclatura, e o da direita é o isômero trans, indicado pela letra E.
Sexto exemplo
Agora são mostrados dois diastereômeros, onde as semelhanças em suas estruturas são observadas, mas pode-se ver que elas não podem se sobrepor.
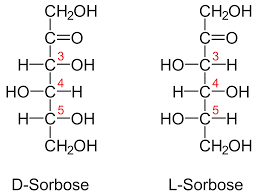
Sétimo exemplo
Finalmente, duas estruturas de carboidratos que são isômeros ópticos chamados enantiômeros são observadas. O da esquerda é dextrógiro, porque polariza o plano da luz para a direita. Por outro lado, o da direita é levógiro, porque polariza o plano de luz para a esquerda.
Referências
- Isômeros (2018). Wikipedia Recuperado de en.wikipedia.org
- Chang, R. (9a ed) (2007). Química Cidade do México, México: Editorial Interamericano da McGraw-Hill.
- Sharma, RK (2008). Estereoquímica – Volume 4. Recuperado de books.google.co.ve
- North, M. (1998). Princípios e aplicações da estereoquímica. Recuperado de books.google.co.ve
- Staff, E. (sf). Fatos rápidos sobre química orgânica: nomenclatura e isomerismo em compostos orgânicos. Recuperado de books.google.co.ve.
- Mittal, A. (2002). Química objetiva para entrada iluminada. Recuperado de books.google.co.ve